Faasidiagrammi
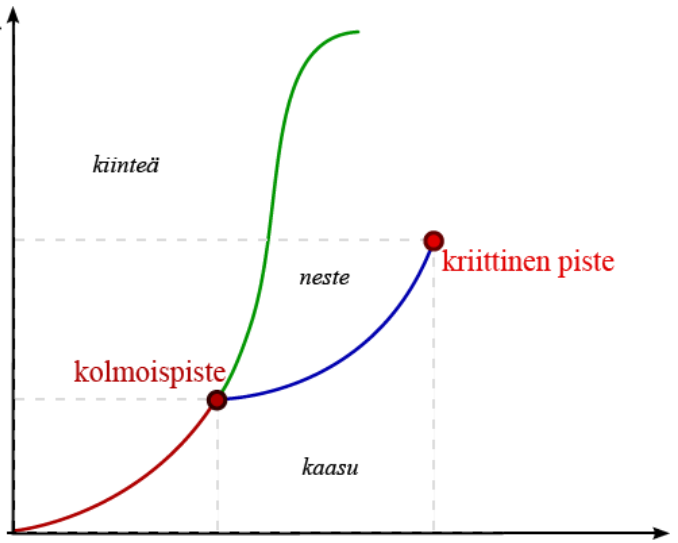
Faasikaavio kuvaa aineen eri olomuotoja (T, p) -koordinaatistossa
T
p
CC BY SA 3.0 CC BY SA 3.0 Matthieumarechal http://en.wikipedia.org/wiki/File:Phase-diag2.svg
Faasikaavion avulla voidaan
ennustaa mitä aineelle tapahtuu
lämpötilan, paineen tai molempien
muuttuessa.
Faasidiagrammi

Eri olomuotoja rajaavat tasapainokäyrät:
- sublimoitumiskäyrä
- höyrystymiskäyrä
- sulamiskäyrä
T
p
CC BY SA 3.0 CC BY SA 3.0 Matthieumarechal http://en.wikipedia.org/wiki/File:Phase-diag2.svg
Tasapainokäyrällä kaksi olomuotoa ovat tasapainossa keskenään eli molemmat olomuodot esiintyvät yhtä aikaa.
Faasidiagrammi

Kolmoispisteen lämpötilassa ja paineessa kaikki kolme olomuotoa ovat tasapainossa ja aine voi esiintyä yhtaikaisesti kaikissa kolmessa olomuodossaan.
T
p
CC BY SA 3.0 CC BY SA 3.0 Matthieumarechal http://en.wikipedia.org/wiki/File:Phase-diag2.svg
Faasidiagrammi

Höyrystä tulee kaasu kriittisessä pisteessä, jolloin kaasun liike-energia on niin suurta, ettei kaasu tiivisty painetta kasvattamalla.
T
p
Höyrystymiskäyrä päättyy kriittiseen pisteeseen, jota korkeammissa lämpötiloissa ja paineissa nestemäisen ja kaasumaisen olomuodon raja häviää.
Höyry on kaasumaista ainetta, joka voidaan muuttaa nesteeksi kasvattamalla painetta.
Esimerkki

Selitä mitä tapahtuu nuolien 1, 2 ja 3 kuvaamissa prosesseissa.
1.
2.
3.
1. Kiinteä aine sublimoituu,
kun aineen lämpötilaa
kasvatetaan.
2. Kaasu tiivistyy nesteeksi,
kun aineen painetta
kasvatetaan.
3. Kiinteä aine sulaa nesteeksi, kun aineen lämpötilaa
kasvatetaan.
T
p
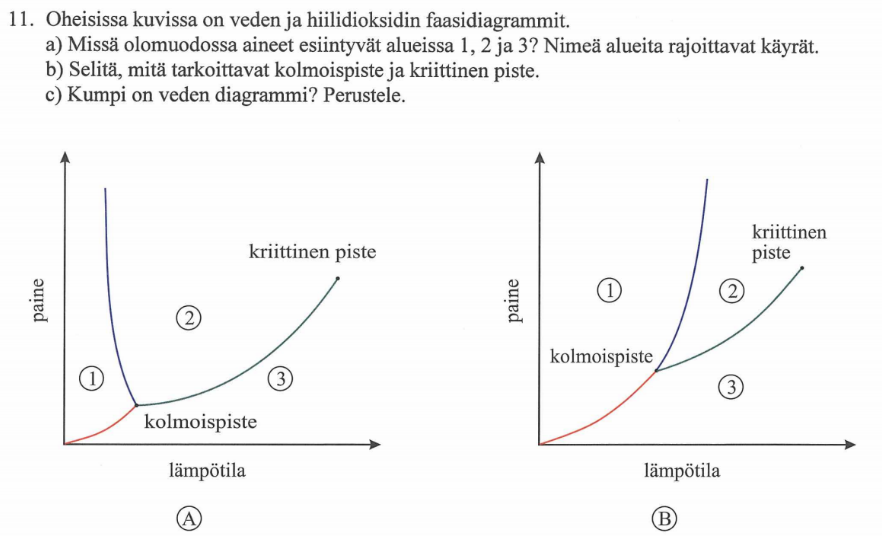
Fysiikan ylioppilaskoe
kevät 2011 tehtävä 11
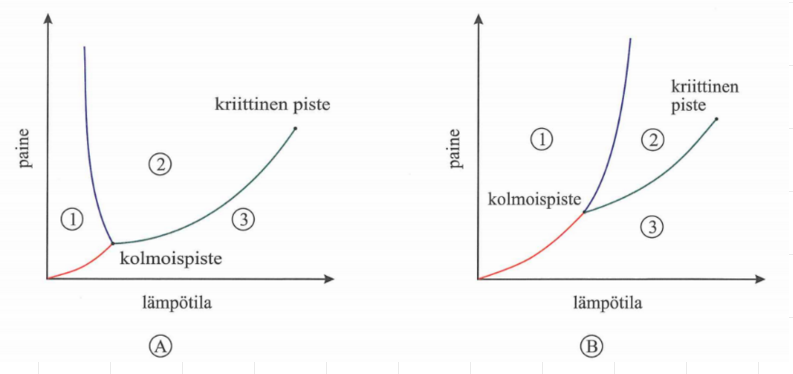
Ratkaisu a-kohtaan
1 Kiinteä, 2 Neste, 3 Kaasu
Sublimoitumiskäyrä, Sulamiskäyrä, Höyrystymiskäyrä

Kolmoispisteen paineessa ja lämpötilassa aine esiintyy kiinteänä, nesteenä ja kaasuna eli kaikki kolme olomuotoa ovat tasapainossa.
Kriittistä pistettä korkeammassa lämpötilassa aine ei enää nesteydy painetta kasvattamalla
Ratkaisu B-kohtaan

Diagrammi A on veden faasidiagrammi.
Vedelle on ominaista, että sulamispistettä vastaava lämpötila laskee paineen kasvaessa.