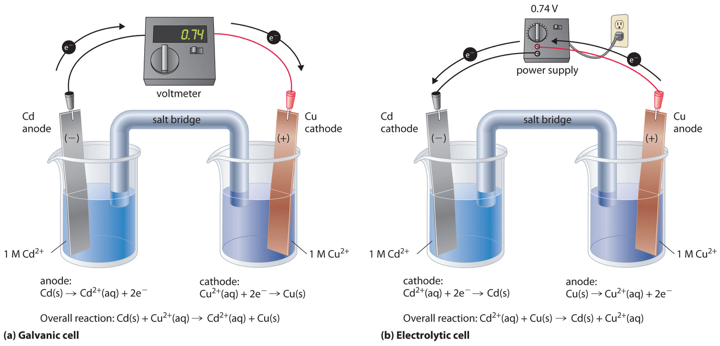
Sähkökemiaa
KE4: Materiaalit ja teknologia 3/5
Metallien jännitesarja
- Jännitesarjalla kuvataan metallien taipumusta muodostaa kemiallisia yhdisteitä
- Metallit on järjestetty pienenevän hapettumiskykynsä mukaisesti, toisin sanoen litium hapettuu paljon helpommin kuin platina.
- Jännitesarjan avulla voidaankin ennustaa, tapahtuuko tietyn metallin ja jonkin toisen metallin ionien välinen hapettumis-pelkistymisreaktio.
- Atomimuodossa oleva epäjalompi metalli pelkistää ionimuodossa olevan jalomman metalli-ionin atomiksi.

R1: Metallien jännitesarja
Suunnitelkaa kokeellinen työ, jolla voidaan määrittää seuraavien metallien paikka sähkökemiallisessa jännitesarjassa
Fe, Sn, Zn, Cu, Ag, Mg, Pb …
R1: Metallien jännitesarja
Mitä kannattaa tutkia?
- Normaalipotentiaaleja tai niiden eroja emme mittaa (turha työ, vie aikaa)
- Kaikkien metallien käyttäytymistä suolahapon (HCl) ei kannata selvittää (miksi?)
- Reaktionopeuden mittaaminen ei ole luotettava mittari jännitesarjan paikkojen määrittämiseksi (mitkä asiat vaikuttavat reaktionopeuteen?)
- Jos ei tapahtunut reaktiota, sekin on tulos!
- Jos ”kirjatieto, taulukkotieto” kertoo toisin, on syytä miettiä virhelähdettä, miksi tulos on erilainen
- Tulosten arviointi: vertailu taulukkotietoinen.
Esimerkki 1: Mitä tapahtuu?
a) sinkin ja hopeanitraatin reaktio
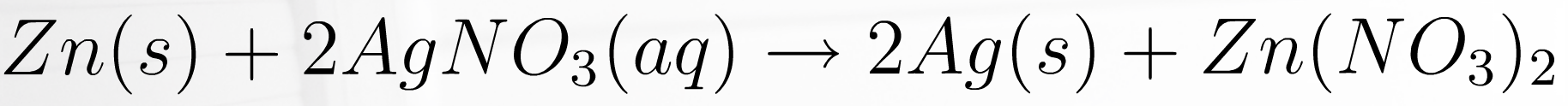
b) kuparin ja sinkkisulfaatin reaktio
epäjalompi metalli atomimuodossa, jalompi ionimuodossa
reaktio
epäjalompi metalli ionimuodossa, jalompi atomimuodossa
ei reaktiota
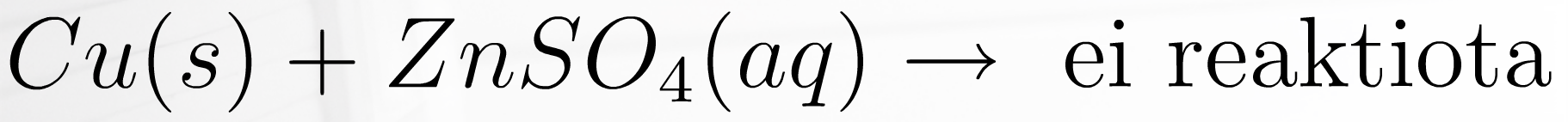
Esimerkki 2: Mitkä seuraavista aineista reagoivat HCl:n kanssa tuottaen vetykaasua?
Cu Zn Mg Ag
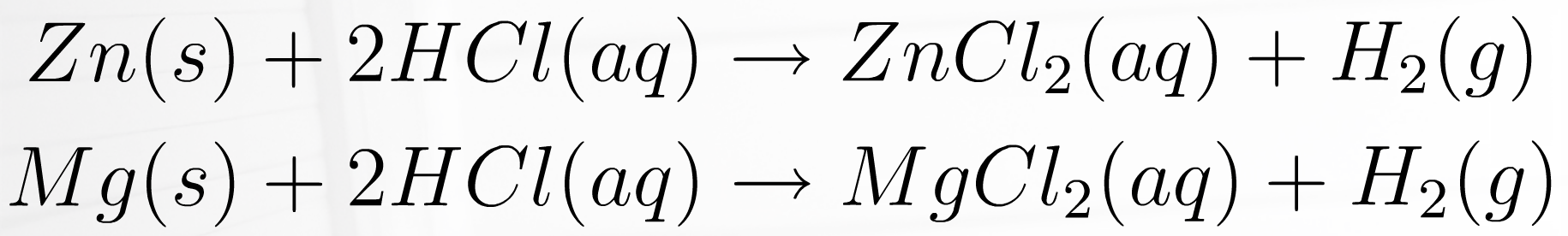
jalot metallit
epäjalot metallit
Normaalipotentiaalit
- Mitkä metallit reagoivat veden kanssa vapauttaen vetyä?
- Mitkä metallit reagoivat happojen kanssa vapauttaen vetyä?
- Miksi jotkin metallit reagoivat vain typpihapon kanssa?
- Onko aina hyvä hapetin vai pelkistin?
Normaalipotentiaalit
- Mitkä metallit reagoivat veden kanssa vapauttaen vetyä?
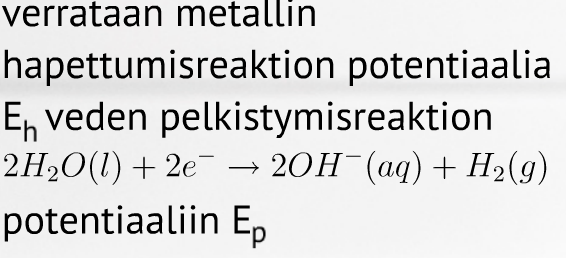
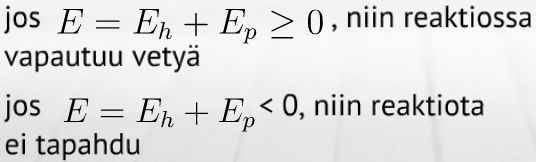
Esimerkki Reagoiko
a) kalsium
b) rauta
vetyä vapauttaen veden kanssa?
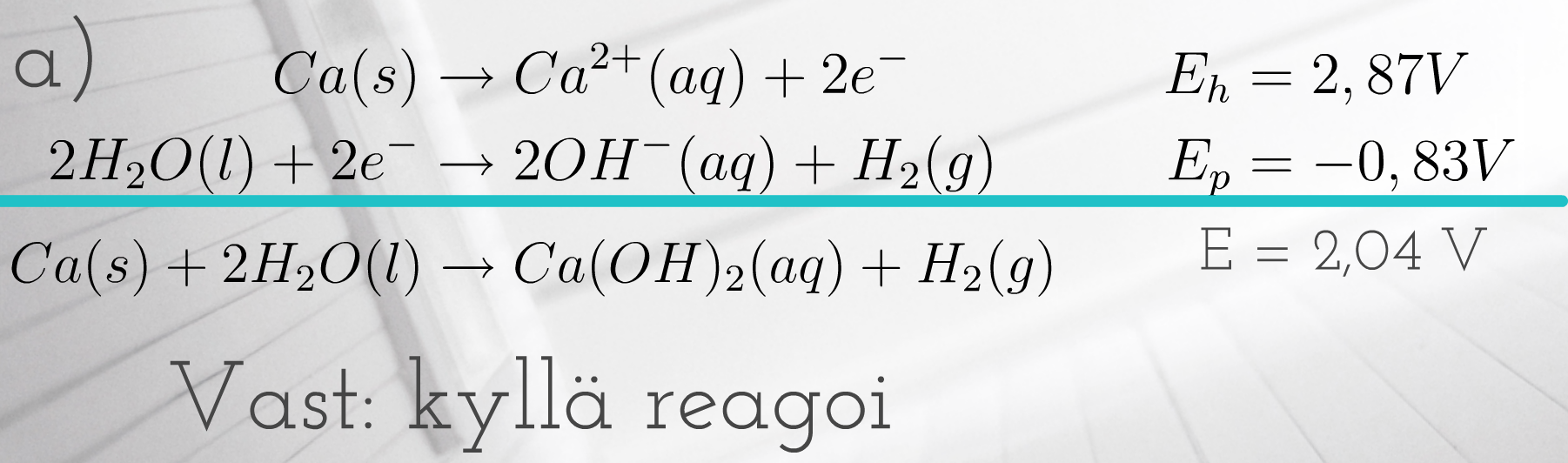
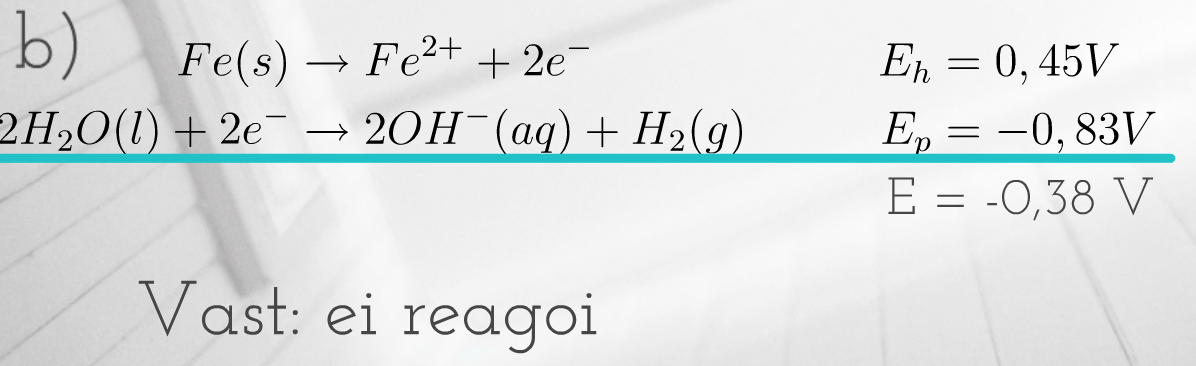
Normaalipotentiaalit
2. Mitkä metallit reagoivat hapon kanssa vapauttaen vetyä?

Jos potentiaalien summa
- E= epänegatiivinen, niin reaktio tapahtuu
- E= negatiivinen, niin reaktiota ei tapahdu
Esimerkki: Osoita normaalipotentiaalien avulla, että lyijy reagoi suolahapon kanssa ja että elohopea ei reagoi.

Normaalipotentiaalit
3. Miksi jotkut metallit liukenevat vain typpihappoon?
Esimerkki: Osoita normaalipotentiaalien avulla, että hopea liukenee typpihappoon.
- typpihapon liuoksessa on vety- ja nitraatti-ioneja, joista vetyionit eivät osallistu reaktioon.
- nitraatti-ionin typpi pelkistyy
- typpihappo voi olla joko väkevää (1) tai laimeaa (2), joten saadaan kaksi pelkistysreaktiota
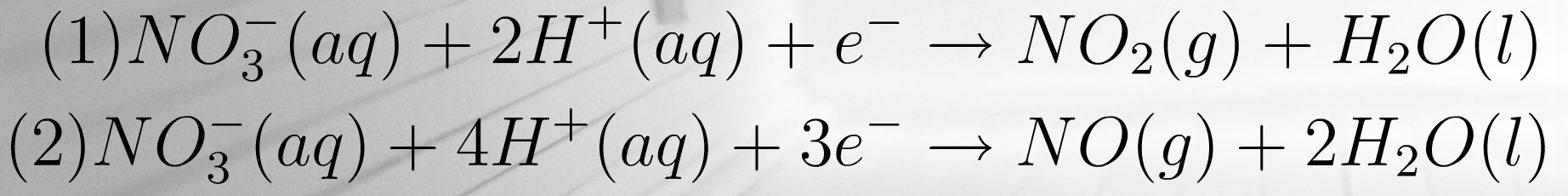
- lasketaan potentiaalien summa ja jos se on epänegatiivinen, reaktio toteutuu

Normaalipotentiaalit
4. Onko aine hyvä hapetin tai pelkistin?
Esimerkki: Perustele pelkistyspotentiaalien avulla, mikä seuraavista on paras hapetin:
- Mitä positiivisempi pelkistysreaktion normaalipotentiaali on, sitä parempi hapetin aine on.
- Mitä negatiivisempi pelkistysreaktion normaalipotentiaali on, sitä parempi pelkistin aine on.
- Aine, jolla on suurempi pelkistyspotentiaalin arvo, voi aina hapettaa normaalipotentiaaliltaan pienemmän aineen, ellei se ole jo hapettuneessa muodossa.
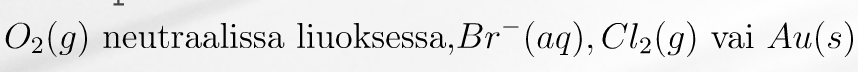

Text
SÄHKÖPARI
Spontaani hapetus-pelkistysreaktio
Sähkövirtaa tuottava hapetus-pelkistysreaktio
Galvaaninen kenno
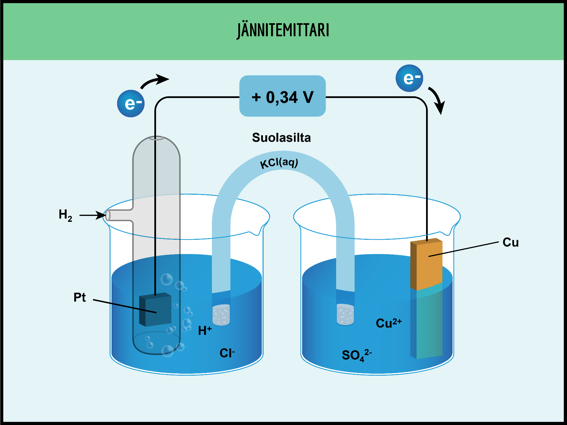
Normaalivetyelektrodi
Pt-elektrodi
elektrolyyttiliuos HCl(aq)
lähdejännite
Normaalipotentiaali-taulukko
kationien kulkusuunta
anionien kulkusuunta
Daniellin pari
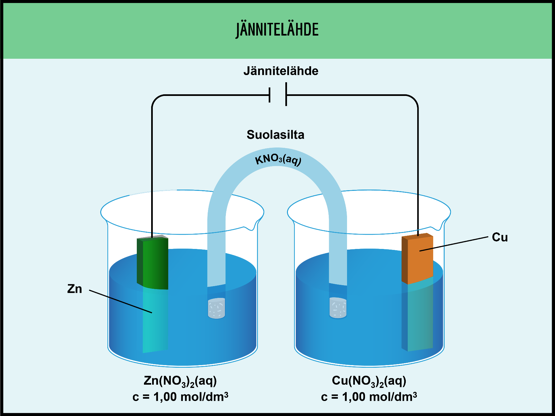
Sähköparien käytännön sovelluksia
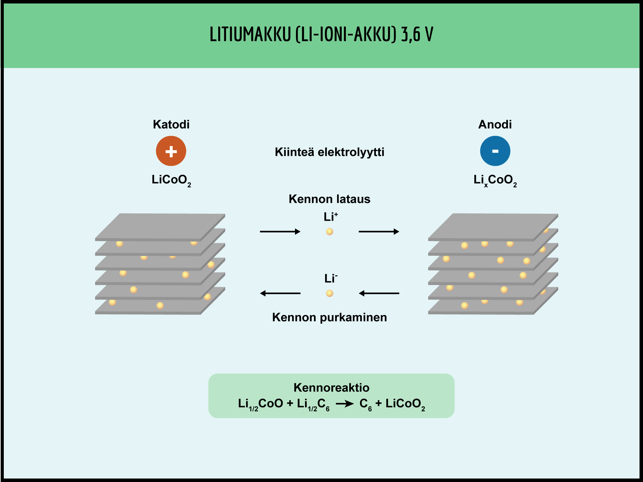
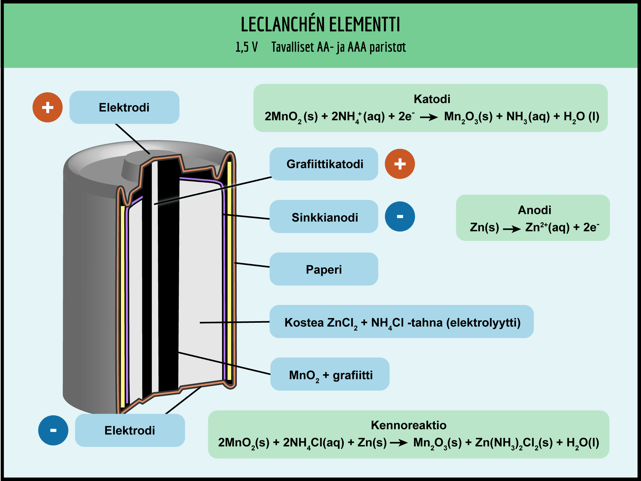
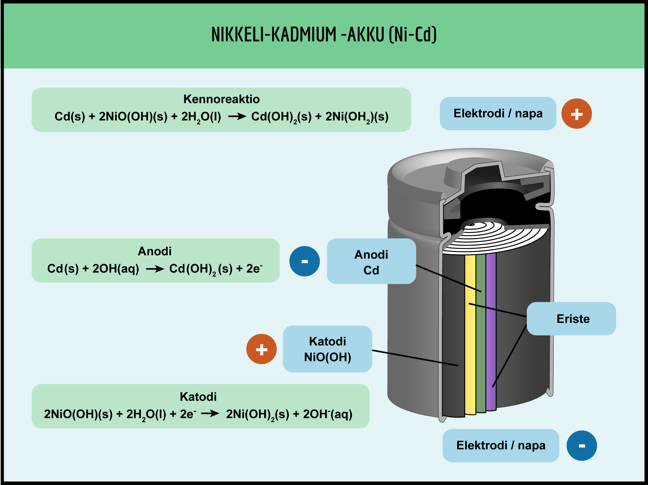
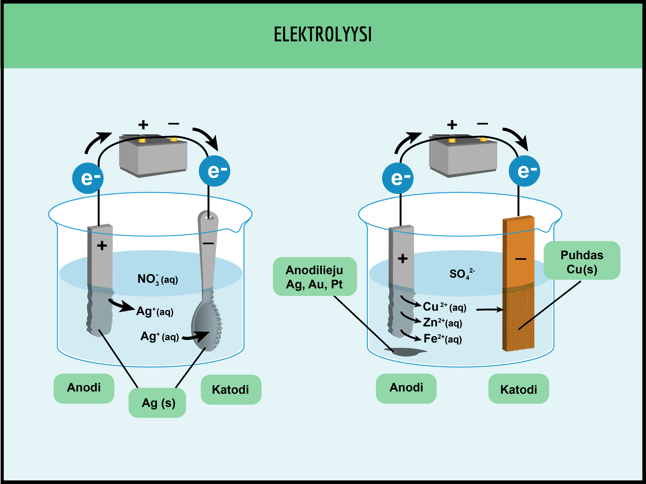
ELEKTROLYYSI
Pakotettu hapetus-pelkistysreaktio
Saadaan aikaan sähkövirralla
YO K2010: Hoffmanin laite ja elektrolyysi laite

Elektrolyysilaskut
Sähkömäärä Q
I = elektrolyysissä käytetty virta (A)
t = elektrolyysiin käytetty aika (s)
n = hapettuvan tai pelkistyvän aineen ainemäärä (mol)
z = siirtyvien elektronien lukumäärä
F = Faradayn vakio
Faradayn vakio
= yhden elektronimoolin varaus
Avogadron vakio
= hiukkasten lukumäärä / mol
elektronin sähkövaraus
Elektrolyysissä muodostuvien aineiden ainemäärät saadaan ratkaistua yhtälöstä:
Esimerkki:
Laske ainemäärä, kun tapahtuma on hopeointi, ja pinnoitus kestää 5 tuntia sähkövirran ollessa 1000 A.
Ratkaisu
I = 1000 A
t = 5 h
n = ?
z = 2
F = 96 485
elektroneja siirtyy 2 kpl
Vastaus: Hopeaa muodostui 93 mol