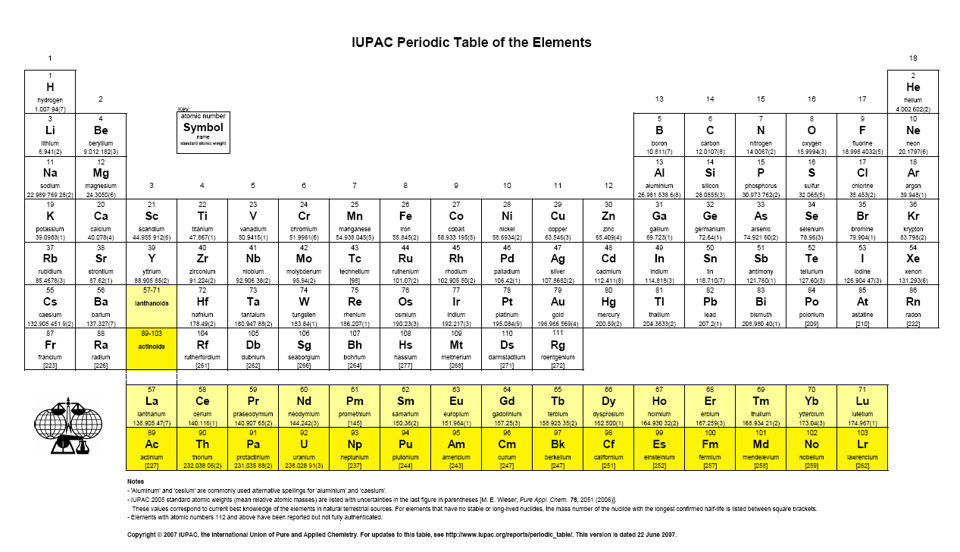
Átomos y periodicidad
¿QUE Y COMO SON LOS ATOMOS?

1855 – Heinrich Geissler (1814 – 1879)
- Produce tubos de vacío
Julius Plücker (1801 – 1868)
- Introduce dos electrodos en los tubos de Geissler y logra hacer pasar una corriente a través de los tubos



http://www.texaswebresources.com/stonevintageradio/images/GEISSLER 3.JPG

1875 – William Crookes (1832 – 1919)
- Construye tubos con mayor vacío respecto a los de Geissler
- La corriente eléctrica se originaba en el cátodo y viajaba hacía el ánodo
- Existía un tipo de radiación que viajaba en línea recta

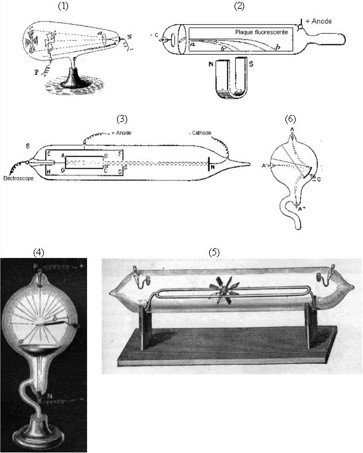
http://members.aol.com/DominiqueCabala/chap5p3.htm

1876 – Eugen Goldstein (1850 – 1930)
- Llama a ese flujo de “radiación”: Rayos catódicos
- Plücker y Crookes demuestran que los rayos catódicos pueden ser desviados por campos magnéticos
¿ Los campos eléctricos los desvían?

1897 – Joseph J. Thomson (1856 – 1940)
- Logra demostrar que los rayos catódicos se desvían en un campo eléctrico
- Logra determinar el cociente entre la carga y la masa para esas partículas.
Los rayos catódicos son corrientes de partículas que transportan carga eléctrica negativa

- Si hasta el momento la masa más pequeña conocida era la del átomo de hidrógeno y la carga más pequeña conocida era la del ion hidrógeno:
Las partículas que constituyen los rayos catódicos:
- Tienen igual masa al átomo de hidrógeno pero transporta mucho más carga que él
- Tiene igual carga al átomo de hidrógeno pero su masa es solo una pequeña fracción del átomo de hidrógeno.

1911 – Robert Andrews Millikan (1868 – 1953)
- Mide la carga eléctrica de las partículas que constituyen los rayos catódicos
- Su masa es 1/1837 la masa del átomo de hidrógeno
- De acuerdo al nombre sugerido por George Stoney se le da el nombre a esa partícula el nombre de electrón
- Se descubre entonces la primera partícula subatómica

1886 – Goldstein
- Realiza experimentos con un cátodo perforado en un tubo de vacío.
- Observa unos rayos que viajaban en sentido contrario a los rayos catódicos: Rayos canal
- 1907 – J.J. Thomson: Confirma que son partículas cargadas positivamente: Rayos positivos.

1914 – Ernest Rutherford (1871 – 1937)
Sugiere que la partícula más pequeña de los rayos positivos, aquella con la masa del átomo de hidrógeno, fuera considerada como partícula fundamental de carga positiva
1920 – Sugiere que la articula positiva fundamental: Protón

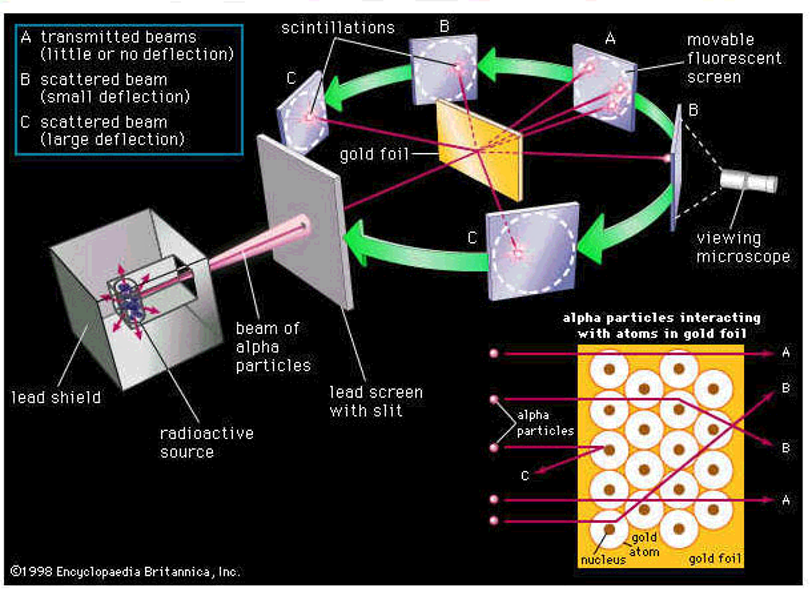
Y la palabra periodicidad

Antigüedad: Nueve elementos:
Edad Media: Cuatro elementos más:
Siglo

Siglo XIX:
- Davy: Alcalinos y alcalinotérreos: nueve
- Gay – Lussac y Thénard: B
- Wollaston: Pd, Rh
- Berzelius: Ce, Se, Si, Zr, Th
- S. Thennand: Os, Ir

Siglo XIX:
- C. Hatchett. Colombio = Nb
- A. Ekeberg: Ta
- L. Vauquelin: Be
- A. Balard: Br
- B. Courtois: I

1830: se conocían 55 elementos
•
¿Cuantos elementos quedan por descubrir?
¿Hay algún límite?
¿Existe alguna relación entre ellos?

¿Existe alguna manera de ordenarlos?
Si existe ¿Qué relación habrá entre ellos?

¿Que implicaron las ideas de Döbereiner 30 años antes de la conferencia de Karlsruhe?



John A. Newlands
(1837 – 1898)

1864 – John A. Newlands (1837 – 1898)
•Ordena los elementos conocidos según sus pesos atómicos crecientes, tal que al disponer los elementos en columnas verticales de siete, los que poseían propiedades semejantes tendían a quedar en la misma fila horizontal

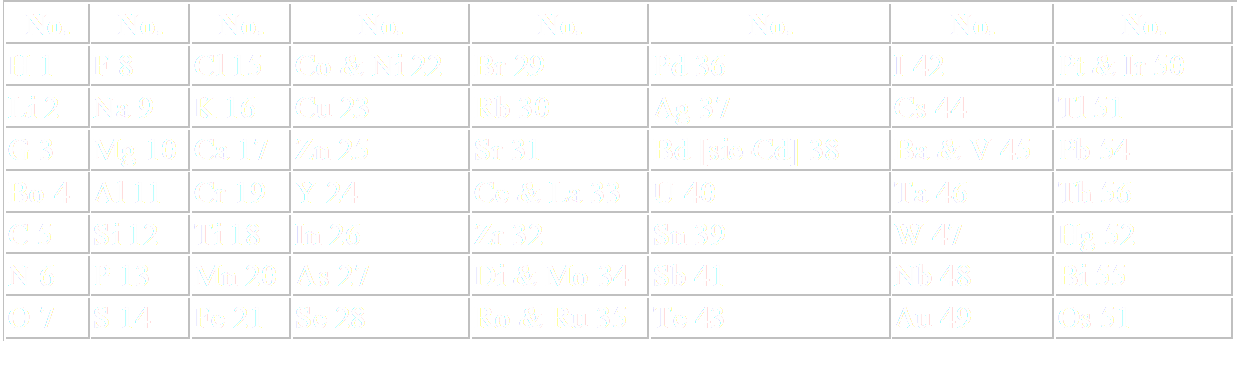


Julius Lothar Meyer
(1830 – 1895)

1870 – Julius Lothar Meyer
- Relaciona los volúmenes atómicos de los elementos en función de los pesos atómicos .
- Encuentra una serie de ondas donde los valores máximos los alcanzaban los metales alcalinos: sodio, potasio, rubidio y cesio

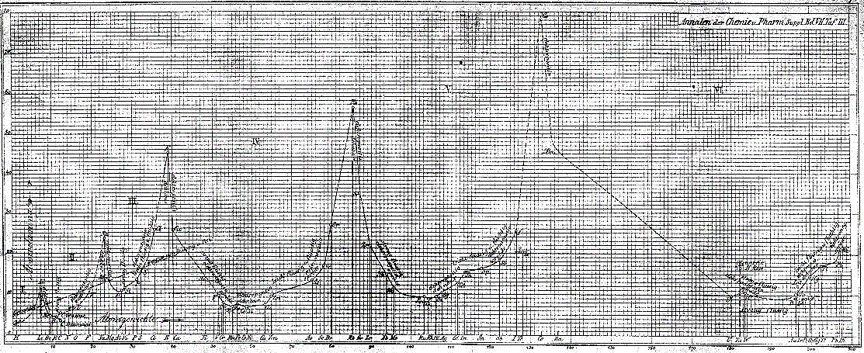

- Segundo y tercer periodos de la tabla de Meyer comprendían siete elementos, octavas de Newlands
- Considerando los periodos entre máximo y máximo no podía forzar la ley de las octavas
- Meyer publica su trabajo en 1870.


Dimitri I. Mendeleiev
(1834 – 1907)

1869 – Dimitri I. Mendeleiev (1834 – 1907)
- Toma como base el concepto de valencia
- Toma como referencia el peso atómico
Observa
- Los primeros elementos presentan una valencia progresiva
- Y esta valencia subía y bajaba estableciendo los periodos




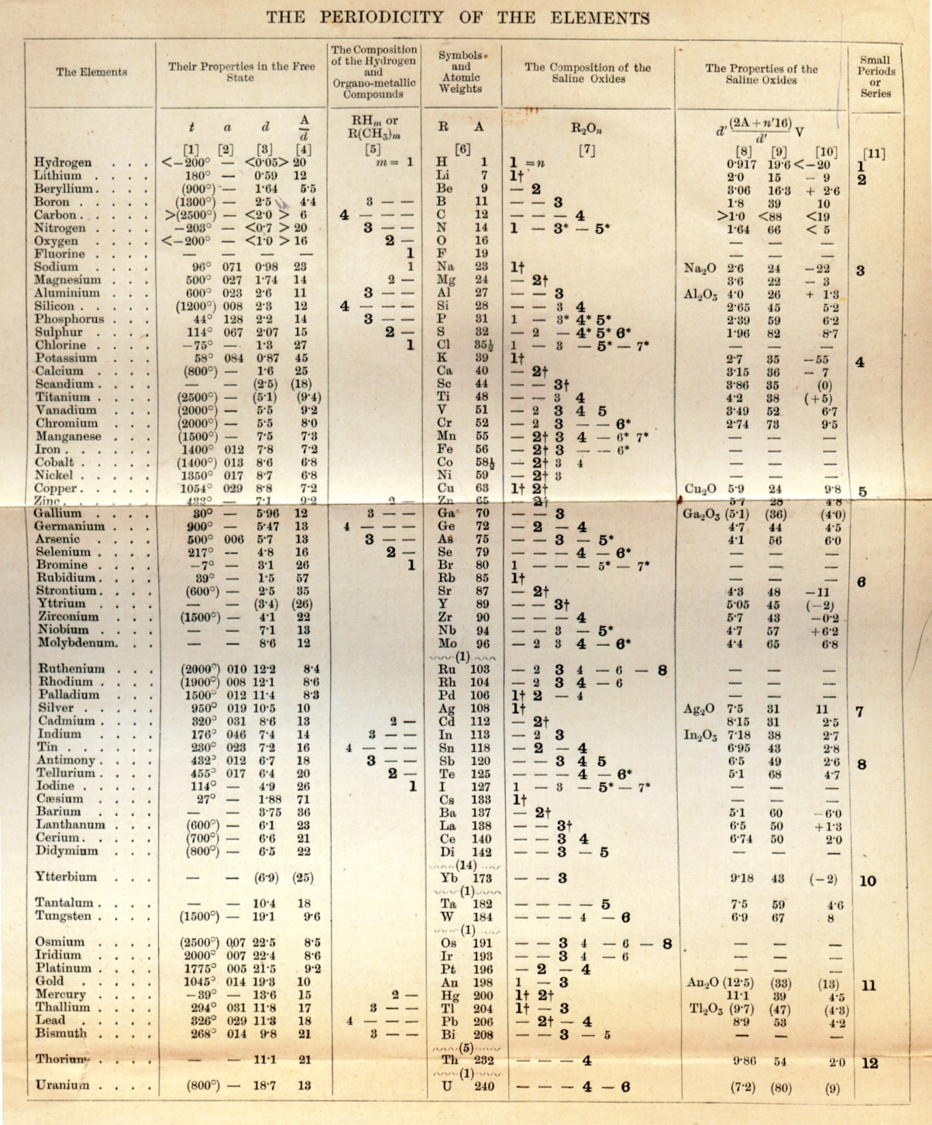

¿Qué caracterizó y le dio supremacía a la tabla de Mendeleiev?
- Deja huecos, en los cuales predice se deben encontrar elementos aún por descubrir:
- eka – aluminio:
- eka – silicio:
- eka – boro:

- Sin embargo, las predicciones de Mendeleiev no siempre fueron correctas:
- Coloca la yodo después del telúro
Si para Mendeleiev era más importante la valencia que el peso atómico ¿donde localizar los gases nobles?

DESCUBRIMIENTO DE LOS ELEMENTOS


Joseph von Fraunhofer

G. R. Kirchhoff


R. W. Bunsen

DESCUBRIMIENTO DE LOS ELEMNENTOS
- 1814, Joseph von Fraunhofer: Experimentando con prismas encuentra que al hacerles pasar luz se formaba un espectro de colores cruzado por una serie de líneas oscuras.
- 1850, G. R. Kirchhoff y R. W. Bunsen: Usan como fuente el mechero de Bunsen para calentar diversos minerales los cuales presentaban un patrón de líneas característico

Espectroscopio
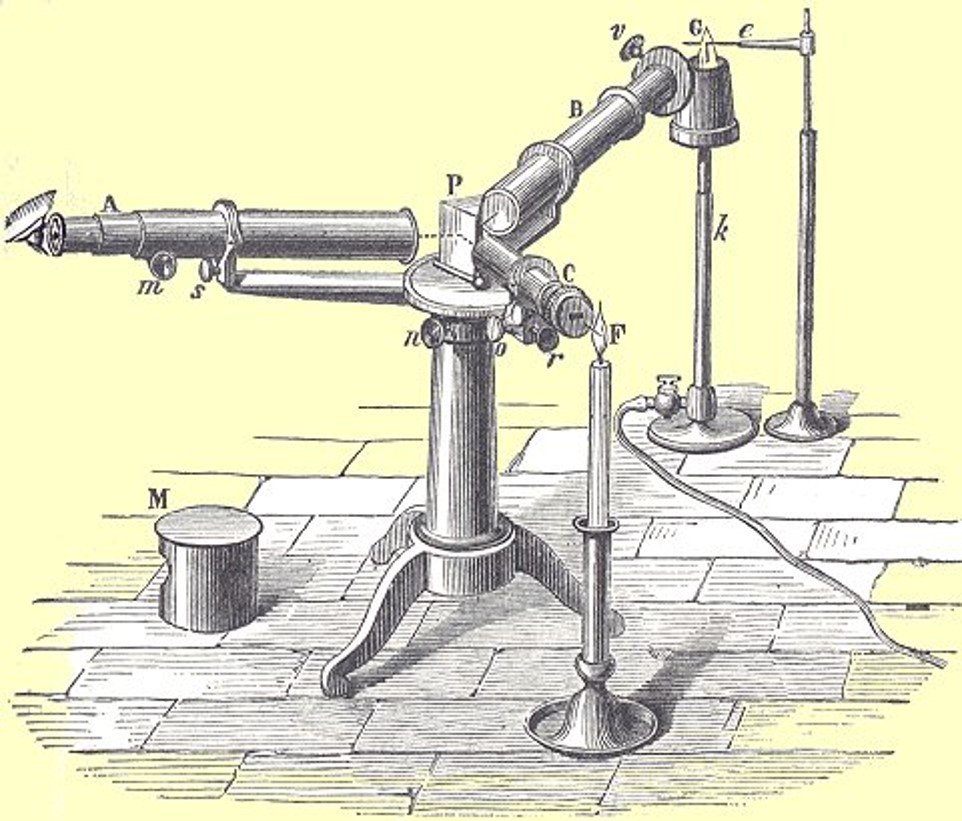





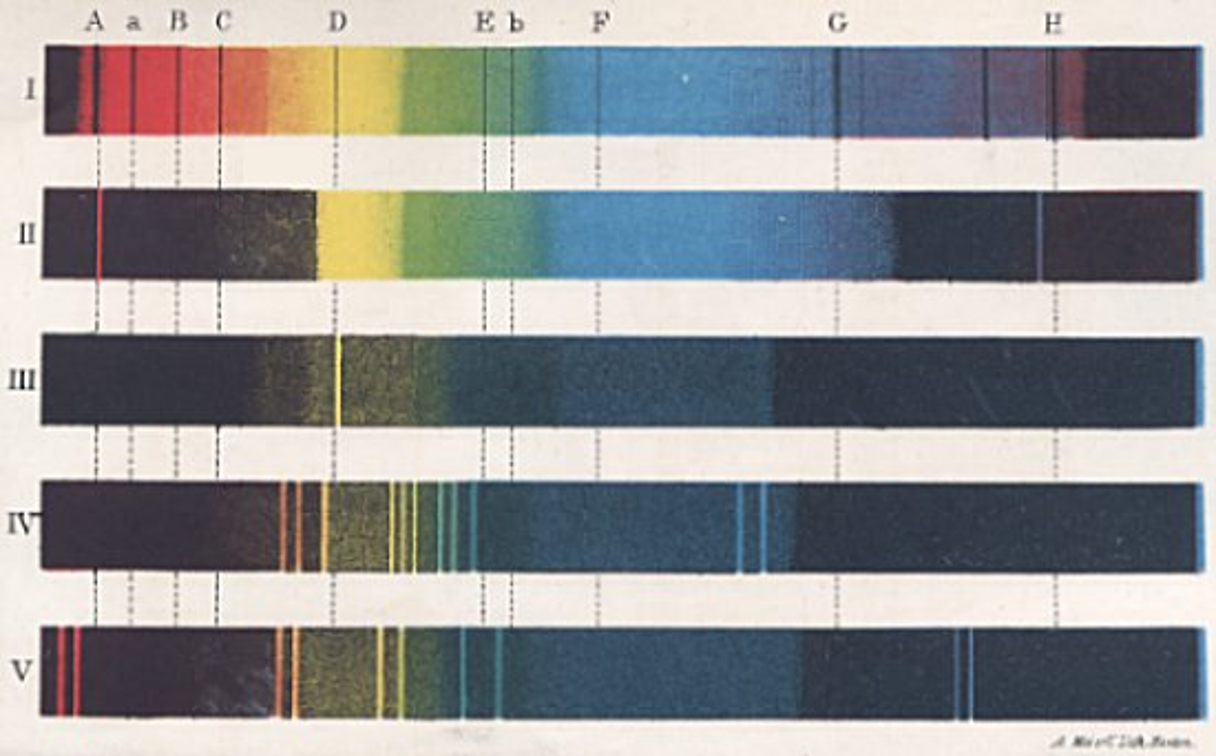

A mediados del siglo XIX se descubren una serie de 14 elementos a los cuales se les da el nombre de tierras raras, las cuales poseían propiedades químicas muy similares y todas tenían una valencia de 3 y tenían pesos atómicos muy similares.


LOS GASES NOBLES

1894, W. Ramsay: Repite los experimentos de Cavendish, encontrando un gas que no reaccionaba y en el espectroscopio presentaba líneas que no correspondían a ningún elemento conocido el cual constituía el 1% del volumen de la atmósfera: descubre el argón
1895, Se estudia el espectro del sol y se descubre un elemento nuevo el Helio, el cual era el mismo encontrado a partir de minerales de uranio
1898, Ramsay: hierve aire líquido y encuentra el neón, criptón y xenón


LA LEY DE MOSELEY
1911



http://www.scitechantiques.com/Mosley_atomic_number/

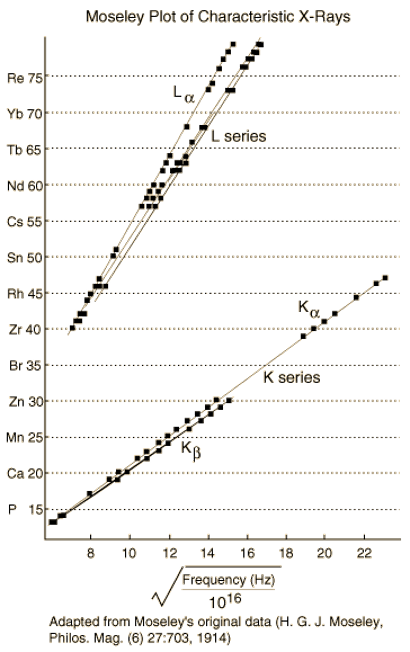
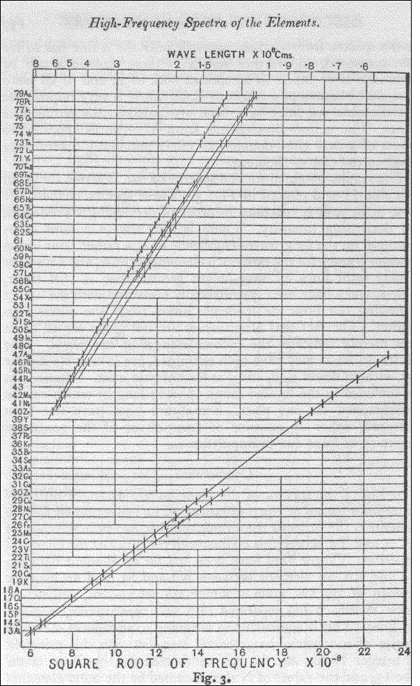

“Es evidente que Q [una función espectroscópica de la frecuencia] aumenta en una cantidad constante a medida que pasamos de un elemento al siguiente, siguiendo para ello el orden químico de los elementos de la tabla periódica […] Sin embargo en tanto que Q aumenta uniformemente, los pesos atómicos varian de una manera aparentemente tan arbitraria, por lo que una excepción en su orden parece no tener nada de sorprendente. Tenemos aquí una prueba de que en el átomo hay una cantidad fundamental que va aumentando regularmente a medida que vamos pasando de un elemento al siguiente. Dicha cantidad sólo puede ser la carga ene l núcleo positivo central, de cuya existencia tenemos ya una prueba definitiva…”
Moseley