13 Lämpökoneet
FY03 Energia ja lämpö
Termodynamiikan pääsäännöt
- Termodynamiikan 0. pääsääntö: tasapaino
- Eristetyssä systeemissä eri lämpöiset kappaleet asettuvat lopulta samaan lämpötilaan
- Termodynamiikan 1. pääsääntö: energian säilyminen
- Energiaa ei voida luoda eikä hävittää, vain muuttaa muodosta toiseen
- Sisäenergian muutos ΔU on systeemiin tuodun energian määrä
- Termodynamiikan 2. pääsääntö: entropian kasvu
- Kaikki ajautuu järjestyksestä epäjärjestykseen (entropia eli epäjärjestys kasvaa)
- Termodynamiikan 3. pääsääntö: entropian nollapiste
- Täydellisen kiteen entropia on nolla
- Kaikki toiminta lakkaa absoluuttisessa nollapisteessä
Termodynamiikan 1. pääsääntö
- Systeemiin siirtynyt energia kasvattaa sen sisäenergiaa
- Energia voi siirtyä lämpönä (säteily, johtuminen, kuljettuminen) tai mekaanisen työn kautta (systeemiin kohdistuva voima)
- Sisäenergian muutos havaitaan systeemin lämpötilan tai olomuodon muutoksena
- Termodynamiikan 1. pääsääntö:
- Merkkisäännöt:
- Systeemiin siirtyvä lämpö ja systeemiin tehty työ ovat positiivisia eli Q > 0 ja W > 0
- Systeemistä pois siirtyvät lämpö ja ympäristöön tehty työ ovat negatiivisia eli Q < 0 ja W < 0
- Sisäenergian kasvaessa sen muutos on positiivinen eli ΔU > 0
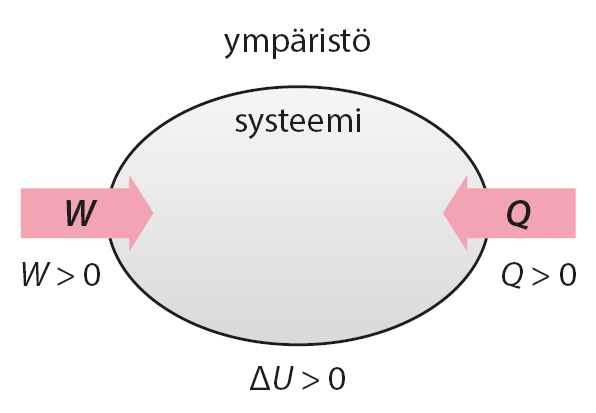
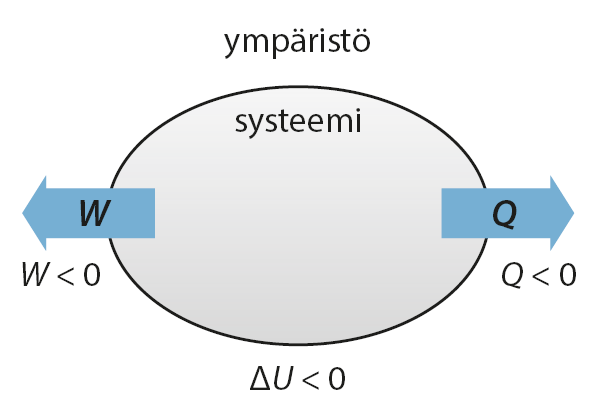
Kuvat: Vipu 3 (Otava)
Esimerkki 1
Kokki valmistaa mannapuuroa pitämällä sitä kuumassa vesihauteessa, jotta puuro ei palaisi pohjaan. Hän sekoittaa puuroa sähkövatkaimella 5 min 30 s saadakseen puuron vaahtoutumaan kuohkeaksi.
Vatkaimen teho on 450 W ja hyötysuhde 42 %. Vesihauteesta puuroon siirtyy lämpömäärä 310 kJ.
Laske puuron sisäenergian muutos.
Puuron sisäenergian muutos on
Puuron lämpötila nousee siihen vesihauteesta johtuvan lämmön ja vatkaimen tekemän työn ansiosta.
Hyötyteho!
Kuinka paljon puuron lämpötila nousee, jos puuroa on 1 kg?
Kaasun tilavuuden muutostyö
- Kun kaasua puristetaan hitaasti kasaan, kaasun lämpötila pysyy vakiona (isoterminen prosessi: pV = vakio, Q < 0)
- Kun kaasua puristetaan nopeasti kasaan, kaasun lämpötila ei ehdi tasaantua ympäristön kanssa (Q ≈ 0)
- Kaasu lämpenee voimakkaasti
- Sylinterin mäntää puristava voima tekee työtä
- Vakiopaineessa mäntää puristavan voiman tekemä työ on
- Kaasun tilavuuden kasvaessa kaasu tekee samansuuruisen työn ympäristöön
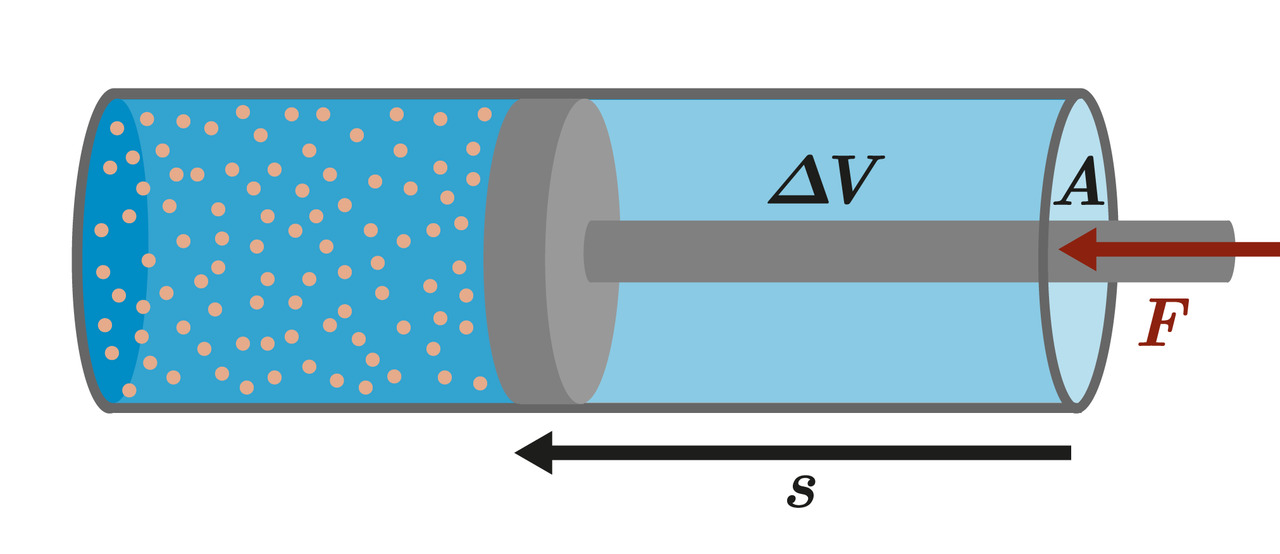
Kuva: Resonanssi 3 (e-Oppi)
1. pääsääntö kaasua puristettaessa
- Isotermisessä tilavuuden muutoksessa kaasun lämpötila ei muutu
- Kaasun sisäenergia ei muutu
- Kaasusta siirtyy tehdyn työn verran lämpöä ympäristöön (Q + W = 0)
- Nopeassa tilavuuden muutoksessa kaasun lämpötila kasvaa
- Osa tehdystä työstä muuttuu kaasun sisäenergiaksi
- Adiabaattisessa tilanmuutoksessa lämpöä ei siirry lainkaan systeemistä ympäristöön (Q = 0)
- Monet ilmakehän prosessit adiabaattisia
| Isoterminen puristaminen | Adiabaattinen puristaminen | |
|---|---|---|
| Työ W | Voima tekee kaasuun työtä, W > 0 | Voima tekee kaasuun työtä, W > 0 |
| Lämpö Q | Lämpöä siirtyy kaasusta ympäristöön, Q < 0 | Lämpöä ei siirry, Q = 0 |
| Sisäenergian muutos ΔU | Lämpötila ja sisäenergia eivät muutu, ΔU = 0 W + Q = 0 | Lämpötila nousee, sisäenergia kasvaa ΔU > 0 |
Esimerkki 2
Vesihöyryä lämmitetään 127 kPa:n vakiopaineessa lämpötilasta 120 °C lämpötilaan 135 °C. Lämmityksen aikana vesihöyry laajenee 380 cm³. Vesihöyryä on 7,0 g, ja sen ominaislämpökapasiteetti on .
Kuinka paljon vesihöyryn sisäenergia muuttuu?
Lämpöopin 1. pääsäännön mukaan
Vesihöyry lämpenee
Vesihöyry laajenee
Kaasuprosessit (V, p)-koordinaatistossa
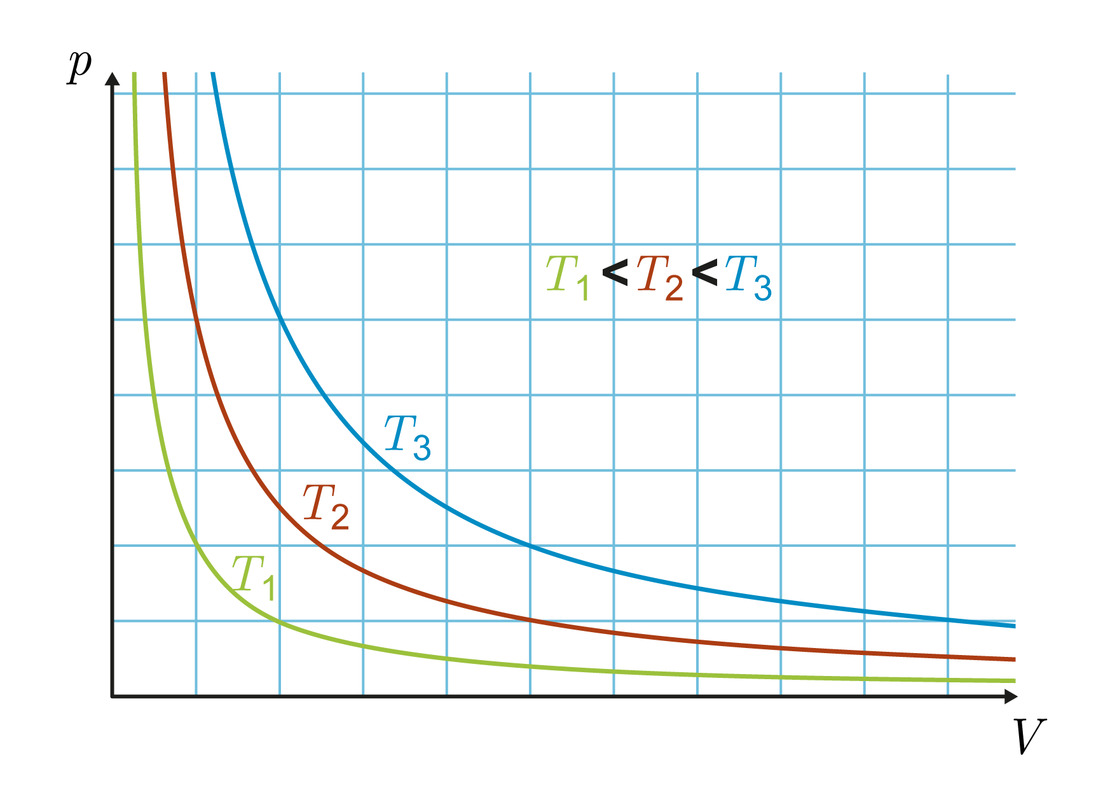
- Isotermisessä prosessissa pV = vakio eli
- Kuvaaja on hyperbeli
- Vakion arvo riippuu lämpötilasta
- Sama esitystapa soveltuu myös muihin prosesseihin
- Kaasun alkutilaa edustaa yksi piste (V, p)-koordinaatistossa ja lopputilaa toinen piste
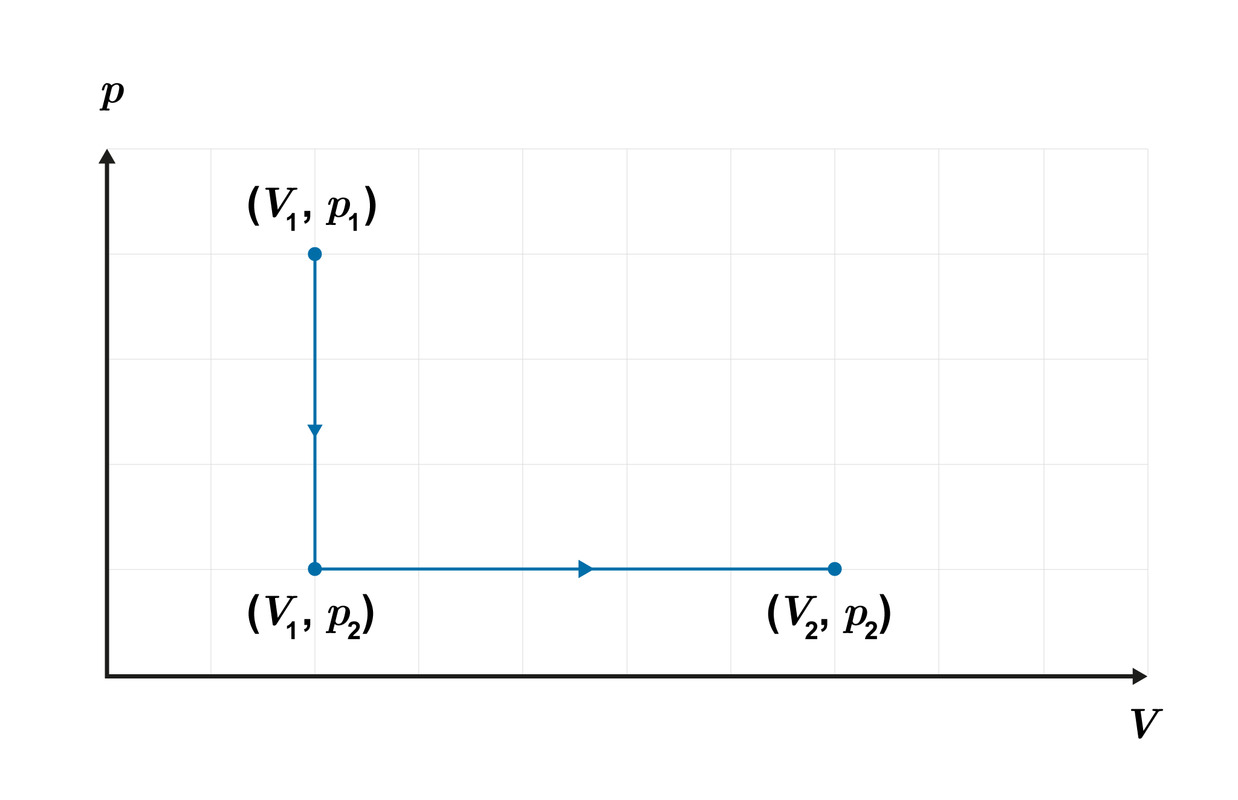
Isokoorinen prosessi
Isobaarinen prosessi
lämpötila laskee
lämpötila nousee
Kuvat: Resonanssi 3 (e-Oppi)
Lämpö energiamuotona
-
Lämpöenergia on energian hyödyttömin muoto
- Sitä voidaan muuttaa työksi vain lämpötilaeroja hyödyntämällä
- Aine virtaa kuumasta kylmään lämpöenergia muuttuu liike-energiaksi
- Ilman lämpötilaeroja ei lämpöenergiaa voi hyödyntää
- Maailmankaikkeus siirtyy kohti tilaa, jossa lämpötila on kaikkialla sama (universumin lämpökuolema)
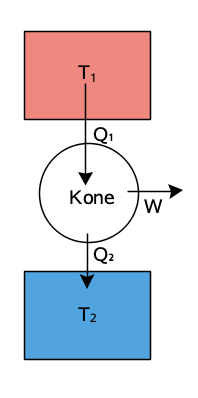
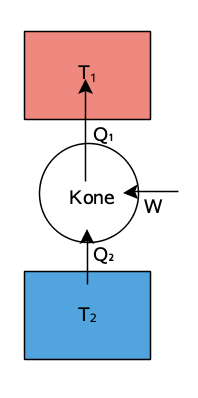
Lämpövoimakone:
lämpöenergiaa siirtyy kuumasta kylmään, osa energiasta muuttuu työksi
Jäähdytin:
tekemällä työtä energiaa voidaan siirtää kylmästä kuumaan
Lämpövoimakone
- Laite, joka tuottaa lämmöstä mekaanista energiaa
- Useimmiten hyödynnetään laajenevan kaasun tekemää työtä
- Kaasua lämmitetään, se laajenee ja tekee työtä
- Kaasun sisäenergia muuttuu mekaaniseksi energiaksi
- Mekaanisella energialla voidaan työntää mäntää tai pyörittää turbiinia
- Laajetessaan jäähtynyt kaasu ohjataan uudelleen lämmitettäväksi
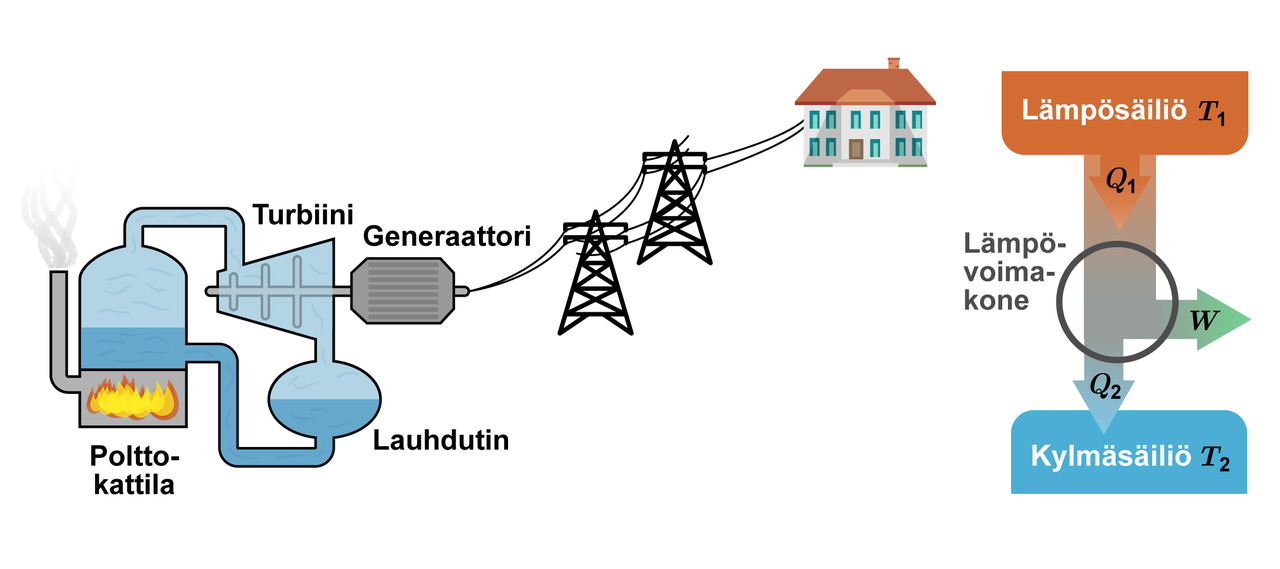
Yläraja noin 60 %
Hyötysuhde:
Kuva: Resonanssi 3 (e-Oppi)
Carnot'n kierto
- Sadi Carnot'n vuonna 1824 keksimä idealisaatio lämpövoimakoneesta, jonka hyötysuhde on mahdollisimman suuri
1–2: Kaasu laajenee isotermisesti, sitoo lämpöä itseensä (W < 0, Q > 0)
2–3: Kaasu laajenee adiabaattisesti, lämpötila laskee (W < 0, Q = 0)
3–4: Kaasu puristuu isotermisesti, luovuttaa lämpöä (W > 0, Q < 0)
4–1: Kaasu puristuu adiabaattisesti, lämpötila nousee (W > 0, Q = 0)
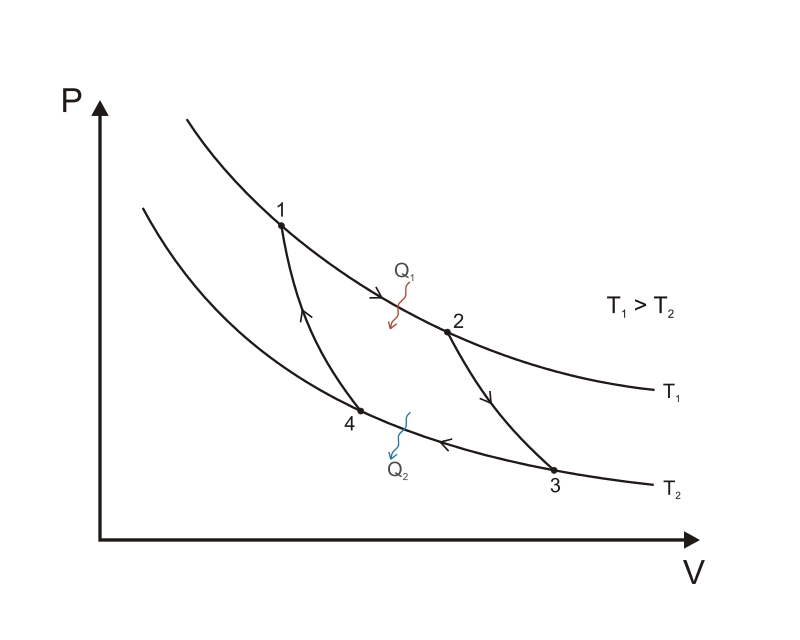
Kuva: Wikipedia
Ideaalisen lämpövoimakoneen hyötysuhde
Lämmönsiirtokone
- Laite, joka siirtää lämpöä kylmäsäiliöstä lämpösäiliöön
- Lämmön siirtämiseksi pitää tehdä työtä
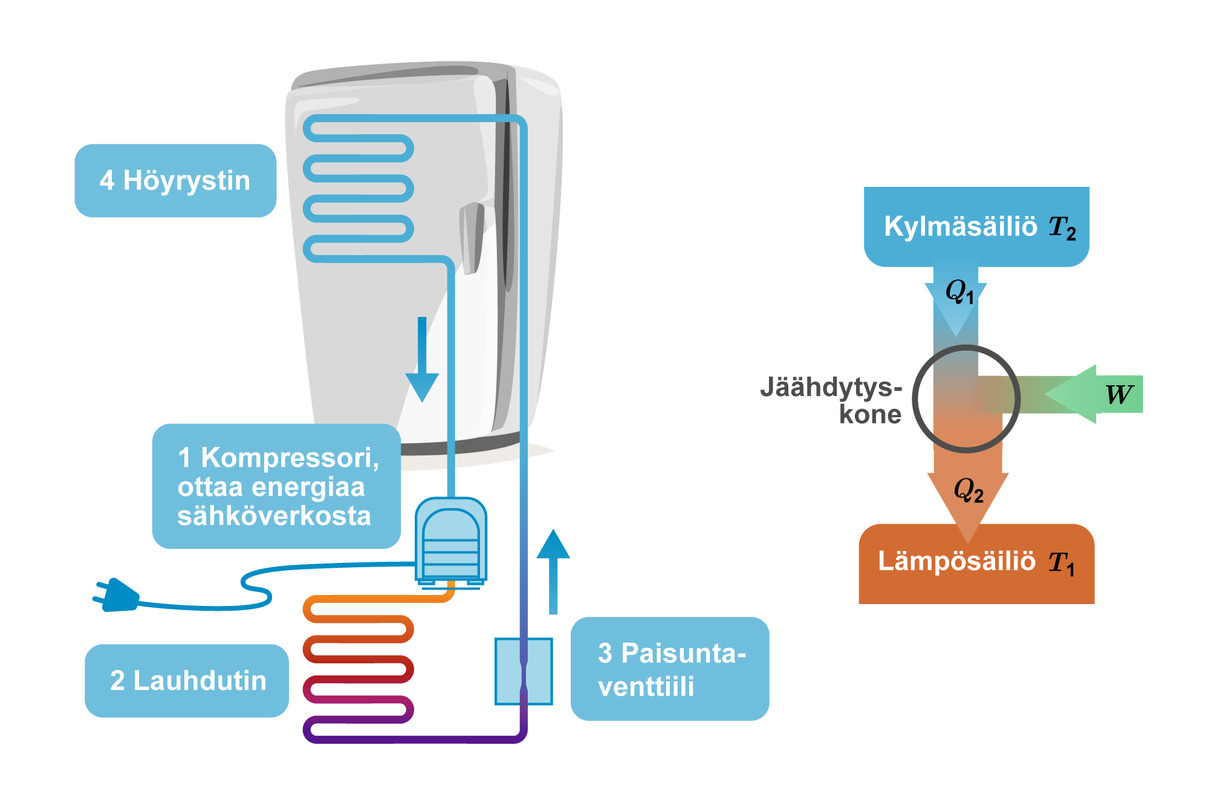
- Jäähdytys perustuu pakotettuihin olomuodon muutoksiin
- Jäähdytysnesteen paineen aleneminen paisuntaventtiilissä (3) saa nesteen höyrystymään
- Höyrystymisessä (4) neste ja laitteen sisäosat jäähtyvät
- Kompressorissa (1) höyry puristetaan uudestaan korkeapaineiseksi nesteeksi
- Nesteytyksessä (2) vapautuu lämpöä, lämpö siirtyy huoneilmaan laitteen takana
Kuva: Resonanssi 3 (e-Oppi)
13 Lämpökoneet
By pauliinak
13 Lämpökoneet
FY03 Energia ja lämpö
- 89



