分子鍵角、極性
22625 劉至軒
Part I
分子的鍵角 (Bond angles)


Bond
Angel
何謂鍵角
就是共價鍵間的角度!
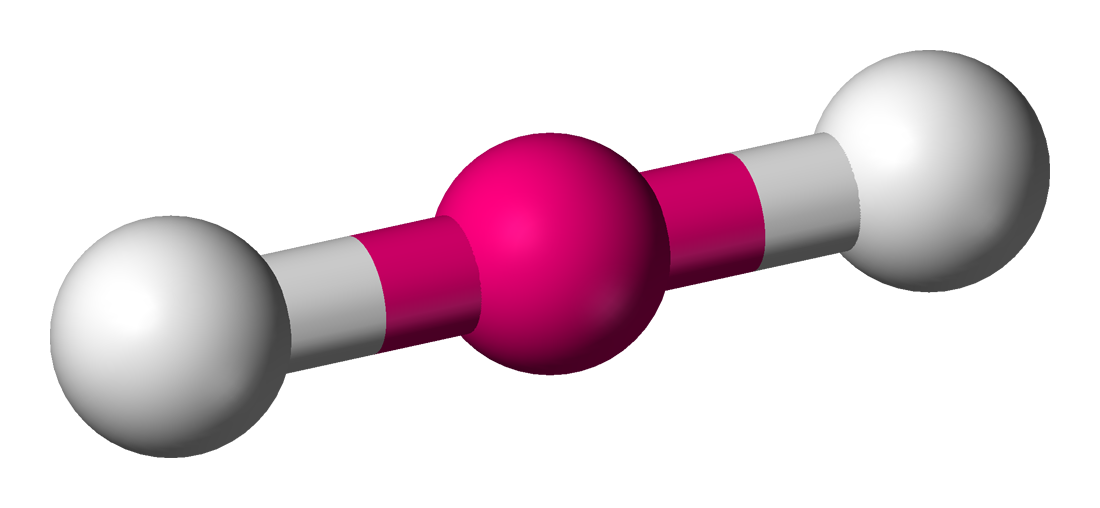
\( \text{CO}_2 \) 分子鍵角:\(180^\circ\)
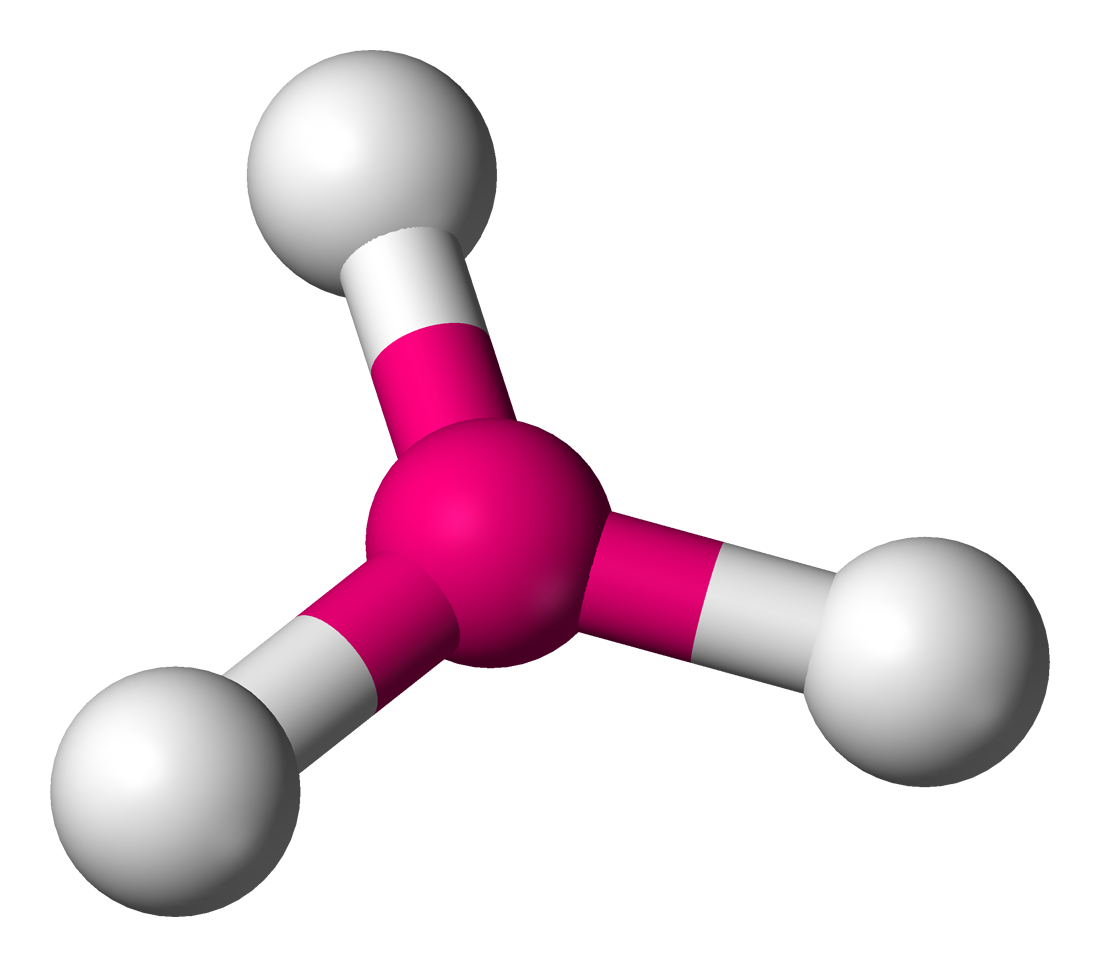
\( \text{BF}_3 \) 分子鍵角:\(120^\circ\)
有哪些罌粟因素影響鍵角?
1. 混成軌域
2. Lone Pair
3. 周圍原子
混成軌域
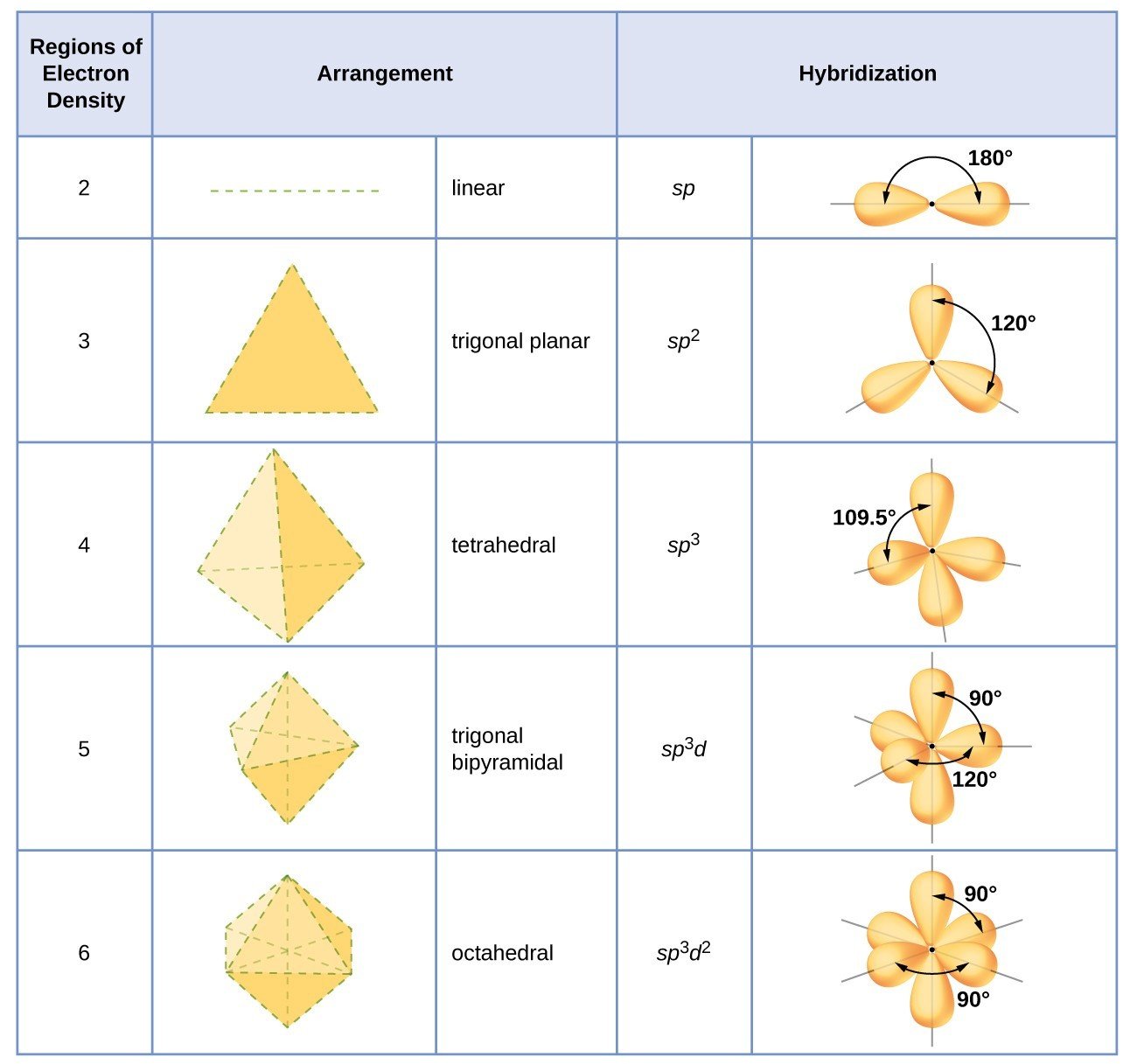
混成軌域

一個原子的\(\text{s}\)軌域和若干個(\(1\)至\(3\)個)\(\text{p}\)軌域形成混成軌域
決定了分子大致的形狀!
到底是\(\text{sp}\)幾?
算一個中心原子的混成軌域為何,大致算其周圍原子數量 + Lone Pair的數量!
到底是\(\text{sp}\)幾?
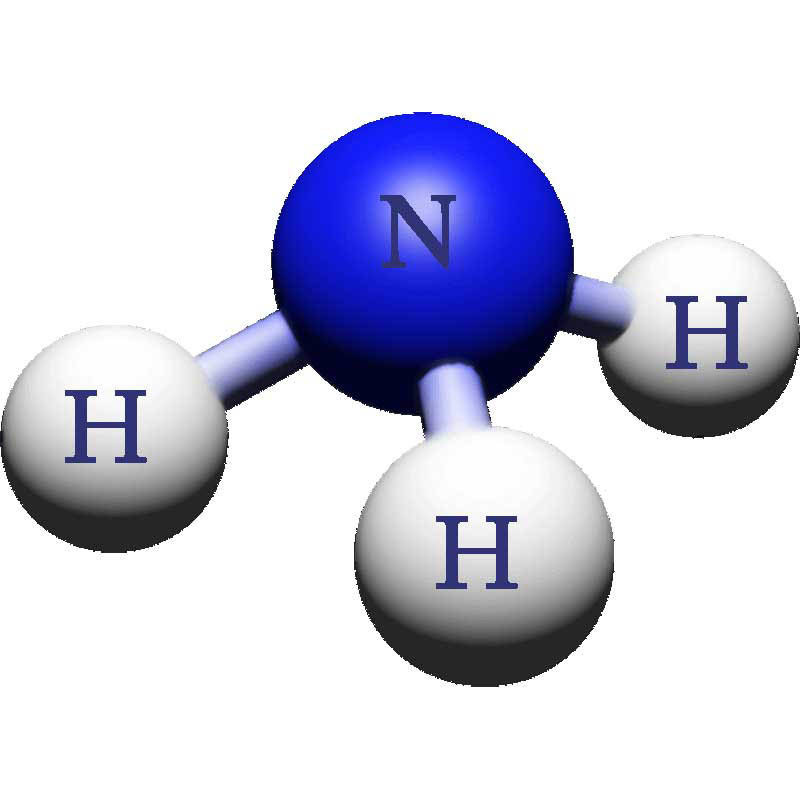
三個周圍原子:
\( \text{sp}^2 \)軌域
到底是\(\text{sp}\)幾?

三個周圍原子 + 一對Lone Pair:\(\text{sp}^3 \)才對!
Lone Pair
電密度超大的微小粒子
來比較壹下

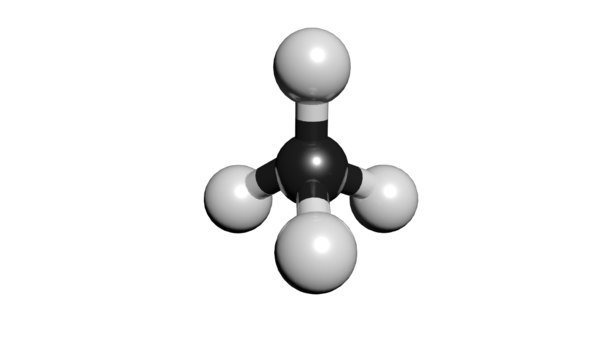
同樣的軌域,不同的鍵角
Lone Pair 搞的鬼!


Lone Pair 搞的鬼!

現象: \( \text{N-H} \)鍵間的鍵角變小了!
解釋:因為最上面有一個LP,為一個電密度很高的負電區,其他原子的電子雲都會排斥
Lone Pair 搞的鬼!

現象: \( \text{N-H} \)鍵間的鍵角變小了!
解釋:因為最上面有一個LP,為一個電密度很高的負電區,其他原子的電子雲都會排斥
歐耨負電
快跑
別過來!
例2:\(\text{H}_2\text{O}\)
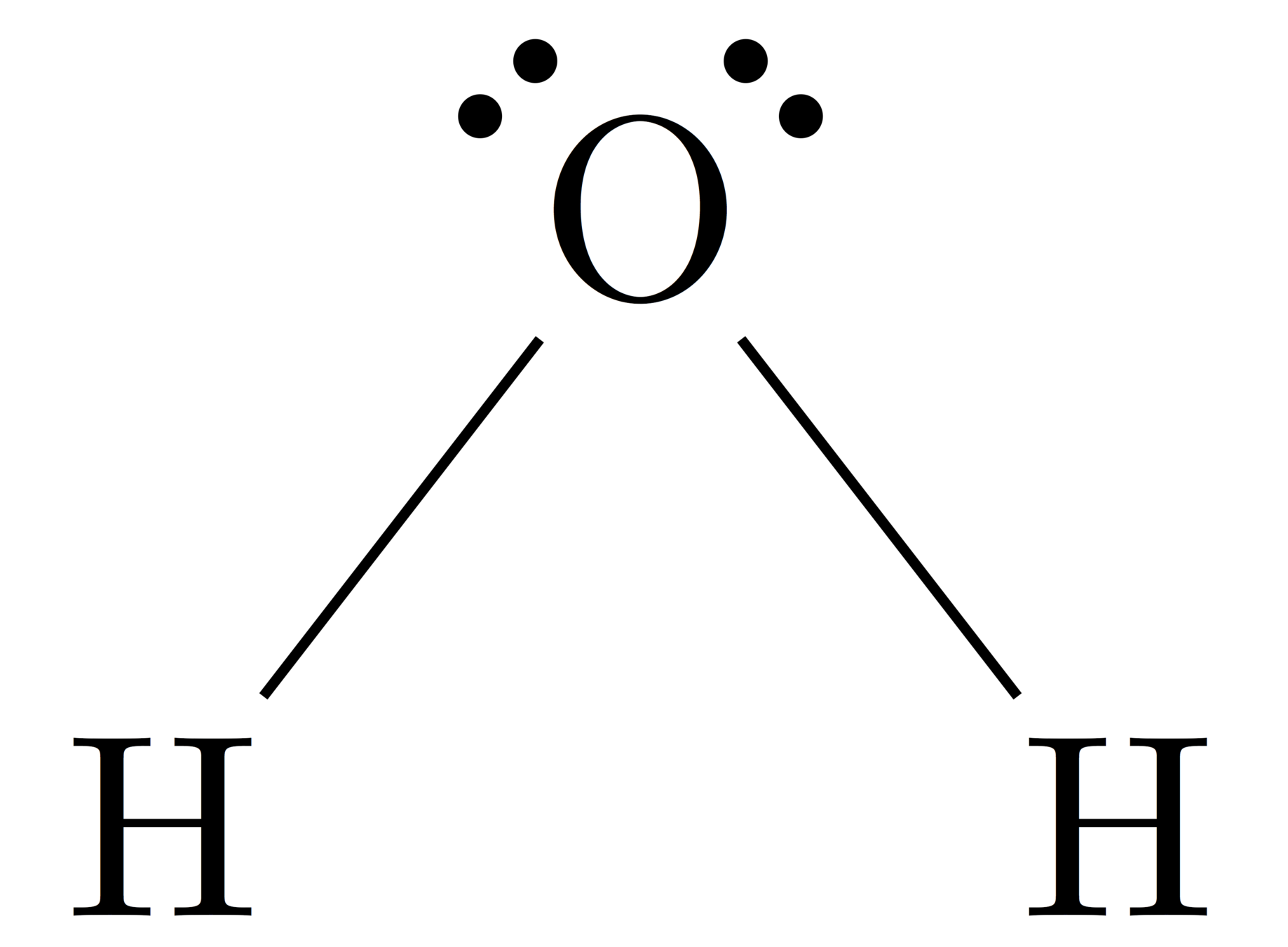
統整:
若中心原子,混成軌域相同,則LP多者鍵角小
VESPR Geometries
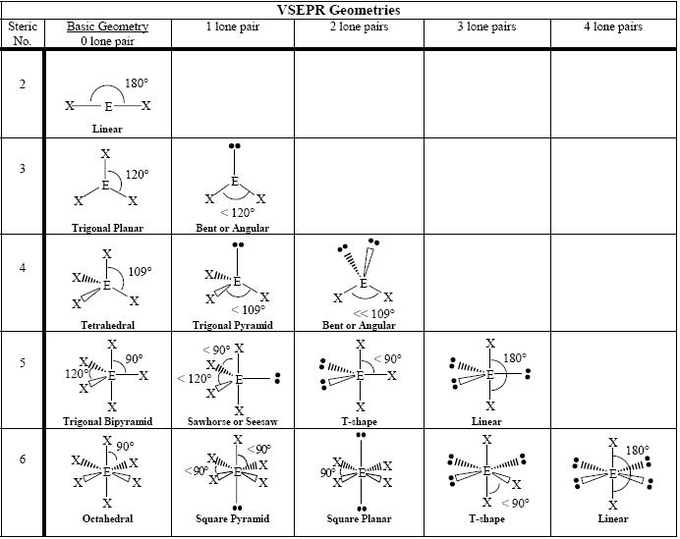
原子差異
\(\text{Cl}、\text{Br}、\text{I} \) 大不同
為什麼原子不同就會影響?
原子達爾文理論?

不是。
電負度!
一個原子多喜歡 \(\text{e}^-\)的度量衡
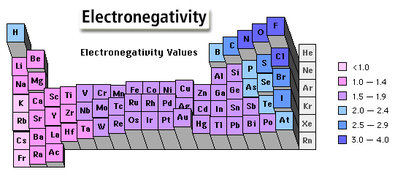
來較量較量
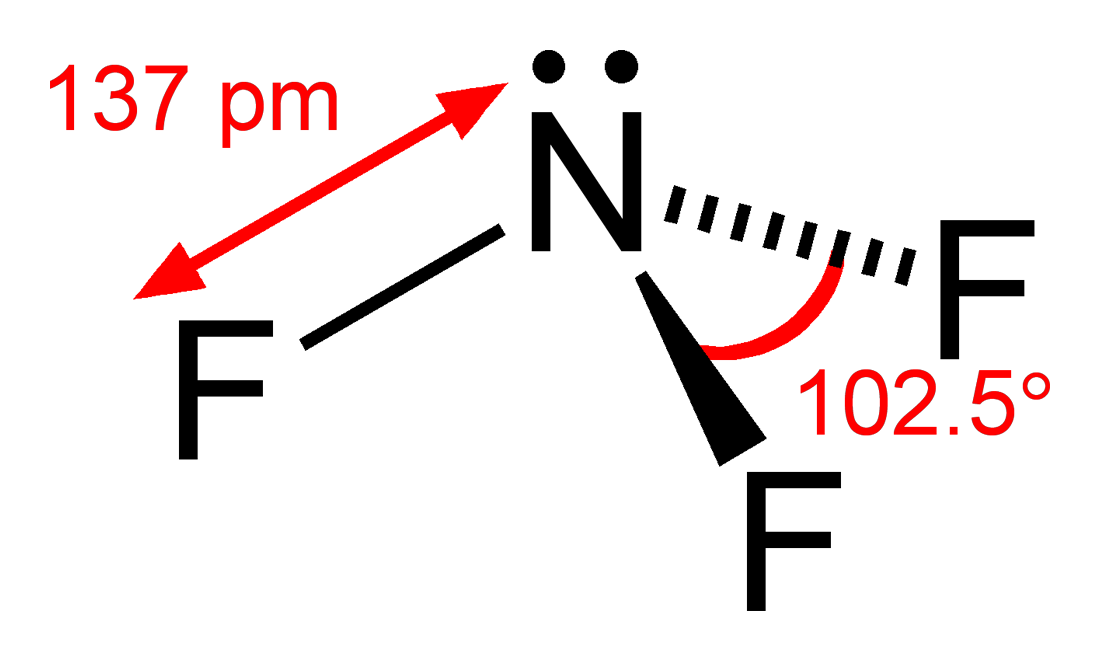
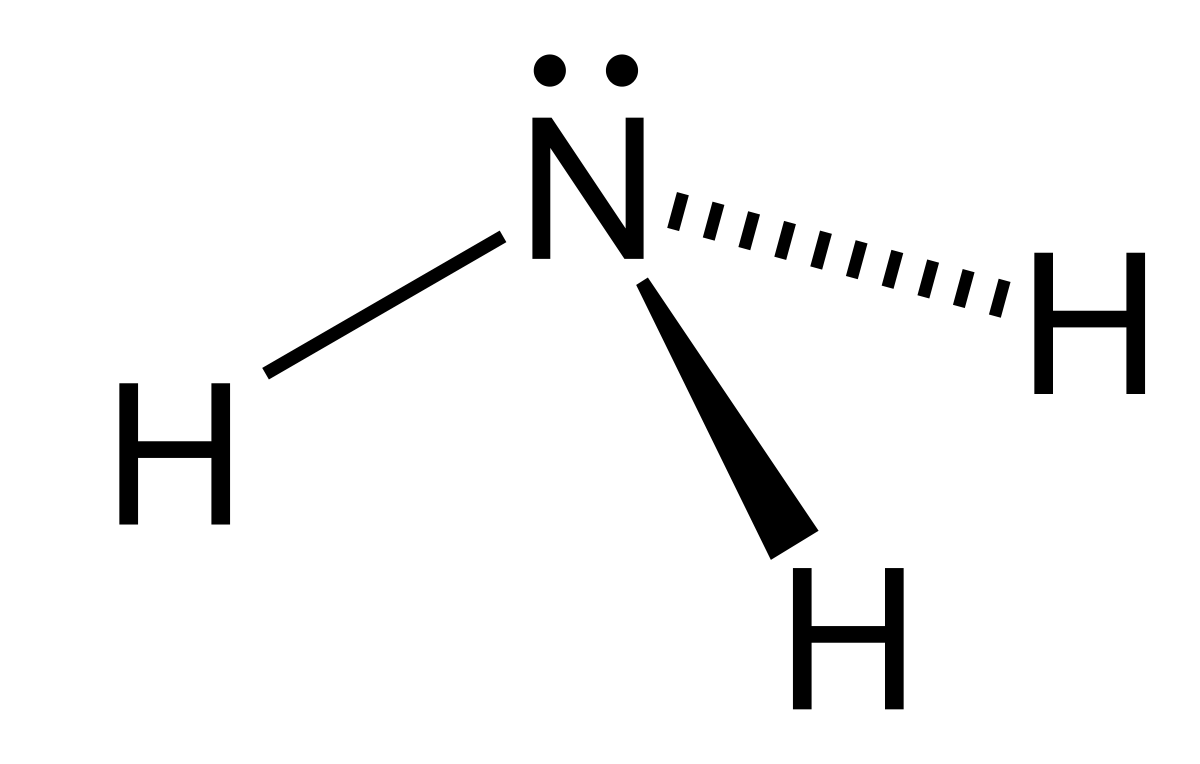
電負度:\(\text{F} > \text{H}\)
所以\(\text{F}\)的電子離中心原子比較遠,鍵角較小
電子會相斥!電子離中心原子越近,鍵角越大。
(中心原子相同的前提之下)
呵呵,化學真有趣
電負度:\(\text{F} > \text{H}\)
所以\(\text{F}\)的電子離中心原子比較遠,鍵角較小?
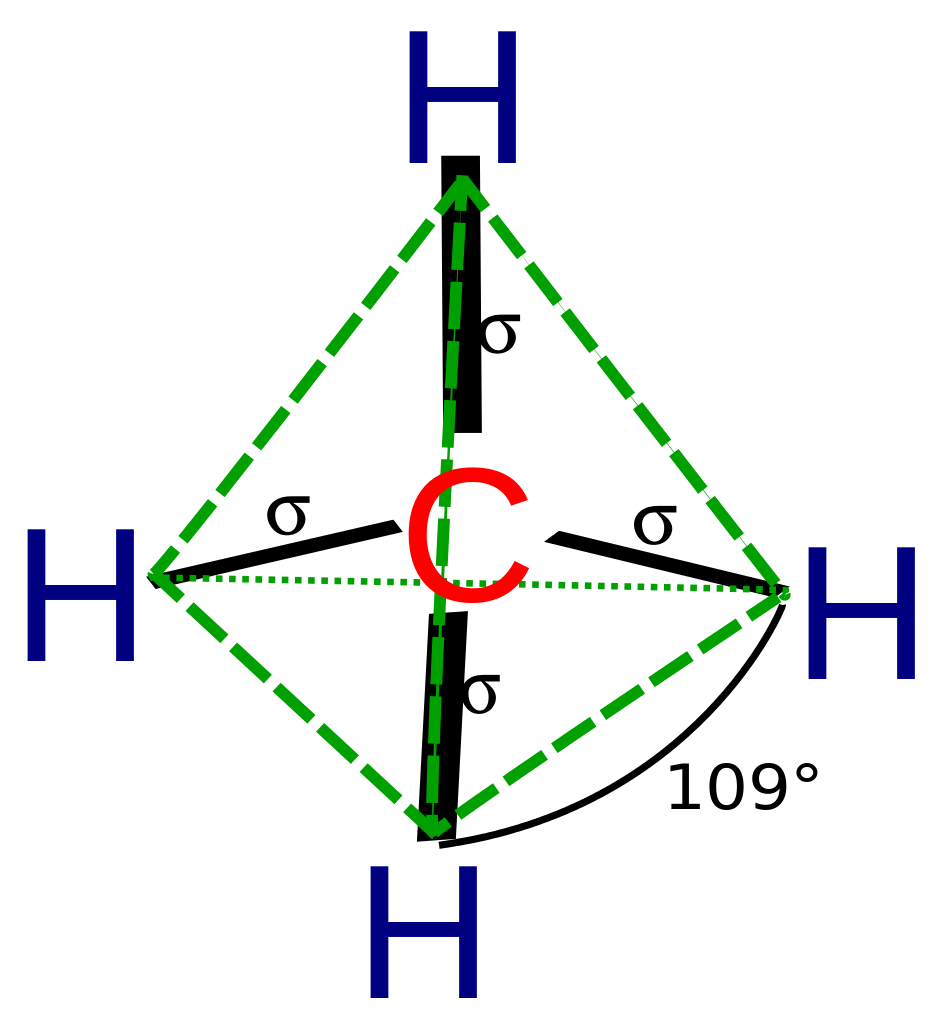
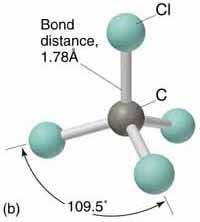
無孤電子對,所以結構不變,相同!
繼續較量較量(中心原子)
其實也是相同概念!中間原子電負度大,則鍵角大。

來排個序吧!
#include <algorithm>
using namespace std;
int N;
vector<int> v;
int main(){
cin >> N;
v.resize(N);
for(int i = 0; i < N; i++) cin >> v[i];
sort(v.begin(), v.end());
for(int x : v) cout << x << " "; cout << endl;
}對不起,錯了
類題
請排序鍵角
\(\text{H}_2\text{O}\)、\(\text{H}_2\text{S}\)、\(\text{CO}_2\)

答案要來嘍
真的要來嘍
真的真的要來嘍
\(\text{CO}_2 > \text{H}_2\text{O} > \text{H}_2\text{S}\)
\(\text{CO}_2 > \text{H}_2\text{O} > \text{H}_2\text{S}\)
直接 \(\text{sp}\) 軌域,沒有Lone Pair,\( 180^{\circ} \)
\(\text{CO}_2 > \text{H}_2\text{O} > \text{H}_2\text{S}\)
直接 \(\text{sp}\) 軌域,沒有Lone Pair,\( 180^{\circ} \)
後兩個\(\text{sp}^3\)軌域,但是\(\text{O}\)的電負度比\(\text{S}\)大,所以電子比較靠近中央,鍵角較大
請比較鍵角
\(\text{NH}_3\)、\(\text{NH}_4^+\)

\(\text{NH}_3> \text{NH}_4^+\)
\(\text{NH}_3> \text{NH}_4^+\)
Lone Pair 的影響比較大,壓爆了其他\(\text{H}\)
Part II
分子的電極性 (Dipoles)
沒有梗啦
為什麼會有電偶極?
原子的本性(電負度)
直接看例子
\(\text{HCl}\)的\(\text{H - Cl}\)鍵雖然是共價鍵,但是\(\text{F}\)的電負度遠大於\(\text{H}\)的電負度,所以電子會比較靠近氟原子,而具有極性
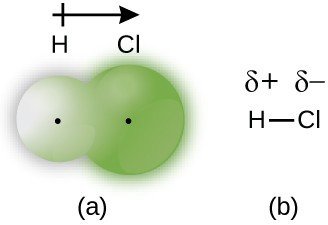
電偶極矩
Electric dipole moment
\(\text{H}_2\text{O}\)的電偶極矩
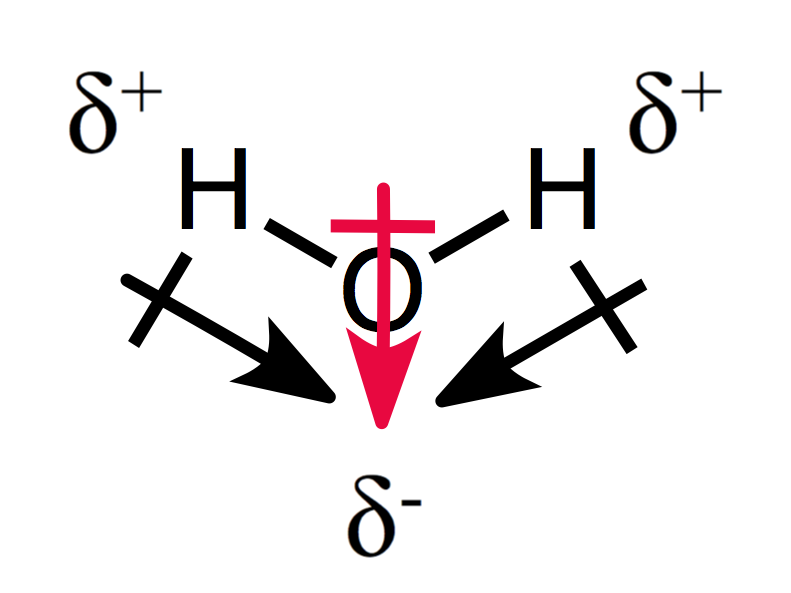
每一個鍵都會有一個電偶極矩,從顛電負度小的指向電負度大的
想像成一個向量
- 大小:與兩個原子的電負度差有關
- 方向:與他們的走向平行
\(\text{H}_2\text{O}\)的電偶極矩

想像成一個向量
- 大小:與兩個原子的電負度差有關
- 方向:與他們的走向平行
向量可以相加!(紅色的箭頭)
帶正電荷的那邊以\(\delta^+\)表示,負電荷以\(\delta^-\)表示
\(\text{H}_2\text{O}\)的電偶極矩

向量可以相加!(紅色的箭頭)
$$ \vec{\mu} = \sum q_i \vec{r_i}$$
- \(\mu\):總電偶極矩
- \(q_i\):第\(i\)個向量的電力(大小)
- \(\vec{r_i}\):第\(i\)個向量的方向
\(\text{O}_3\)的電偶極矩
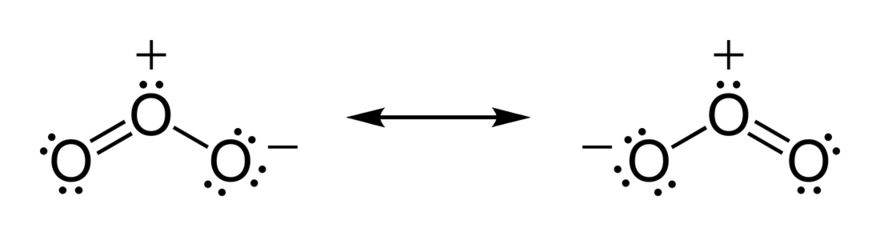
除了共振結構之外,單鍵的那個氧原子帶有比較多電子,相對於中心氧原子帶負電。
氫鍵
極性分子的正極和另外的極性分子的負極會因為電磁力而形成氫鍵
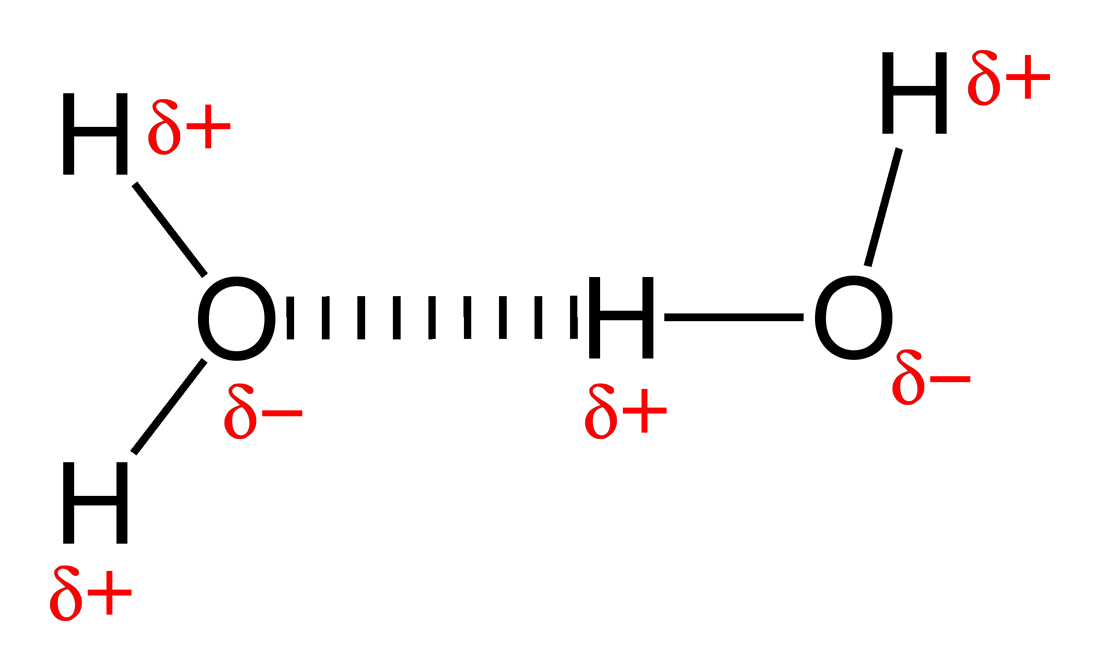
Ex. 1 —— \(\text{H}_2\text{O}\)

Ex. 2 —— \(\text{CH}_3\text{COOH}\)
類題
請畫出四氯乙烯(\(\text{C}_2\text{Cl}_4\))各鍵結的電偶極矩,並計算其電偶極矩合?
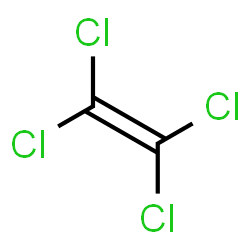


$$ = \vec{0}$$
請問下列何者分子屬於極性分子?(多選)
- \(\text{NH}_3\)
- \(\text{CO}_2\)
- \(\text{BF}_3\)
- \(\text{HCl}\)
- \(\text{CCl}_4\)
請問下列何者分子屬於極性分子?(多選)
- \(\text{NH}_3\)
- \(\text{CO}_2\)
- \(\text{BF}_3\)
- \(\text{HCl}\)
- \(\text{CCl}_4\)
是!為三角錐形\(\text{sp}^3\)上面還有一個孤對電子
不是!為直線型,所以兩個電偶極抵銷
不是!注意,\(\text{BF}_3\)不滿足八隅體,氟原子為正三角形。
是!\(\text{H}\)和\(\text{Cl}\)間就有偶極矩了
不是!\(\text{C}\)和\(\text{Cl}\)間雖然有四個偶極矩,但是因為是四角錐的關係所以抵銷了

謝謝大家的聆聽!準備Kahoot吧!
分子鍵角、極性
By sean5463
分子鍵角、極性
- 130



