Halfgeleiders
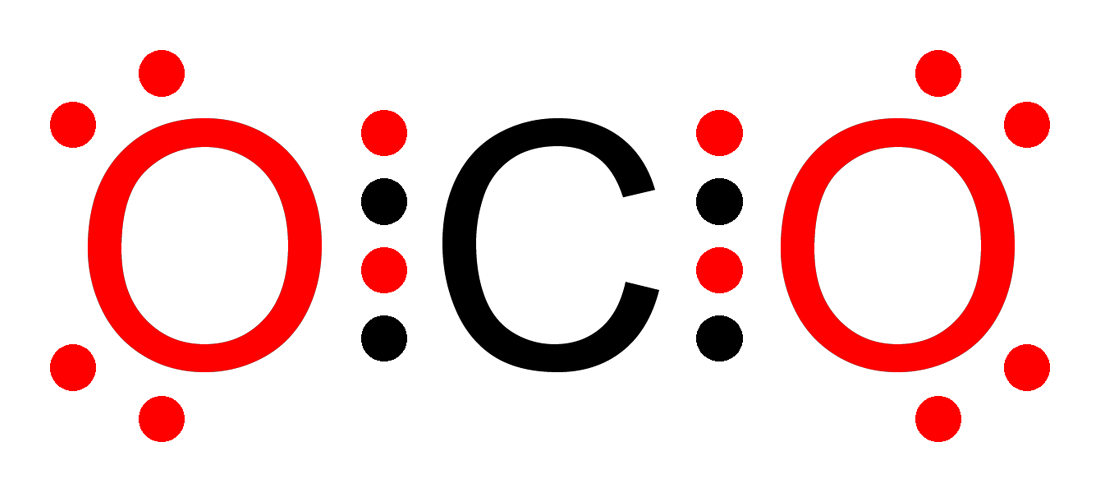

Octetregel voor valentie-elektronen
Octetregel voor valentie-elektronen
Blijft gelden in de meeste VASTE STOFFEN
Octetregel voor valentie-elektronen
Blijft gelden in de meeste VASTE STOFFEN
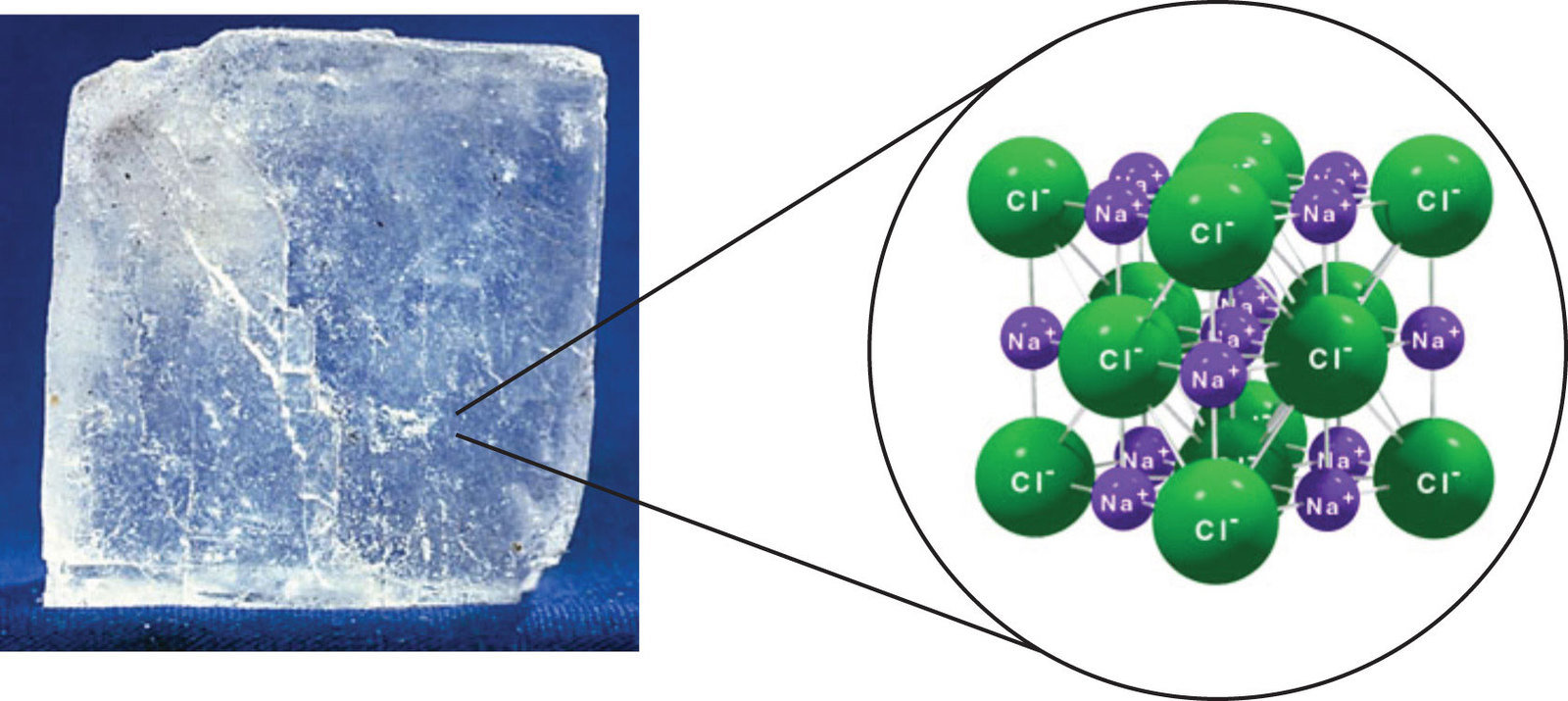
Ionaire vaste stof = Elk atoom heeft 8 VE
vb. NaCl (Cl krijgt het VE van Na, op die manier hebben ze na binding beide 8 VE)

Ionaire vaste stof = Elk atoom heeft 8 VE
vb. NaCl (Cl krijgt het VE van Na, op die manier hebben ze na binding beide 8 VE)

Covalente vaste stof = Elk atoom ook 8 VE
vb. I2 (I met 7 VE, ze gebruiken elk één elektron in een gedeeld elektronenpaar, dus in totaal 8 VE)
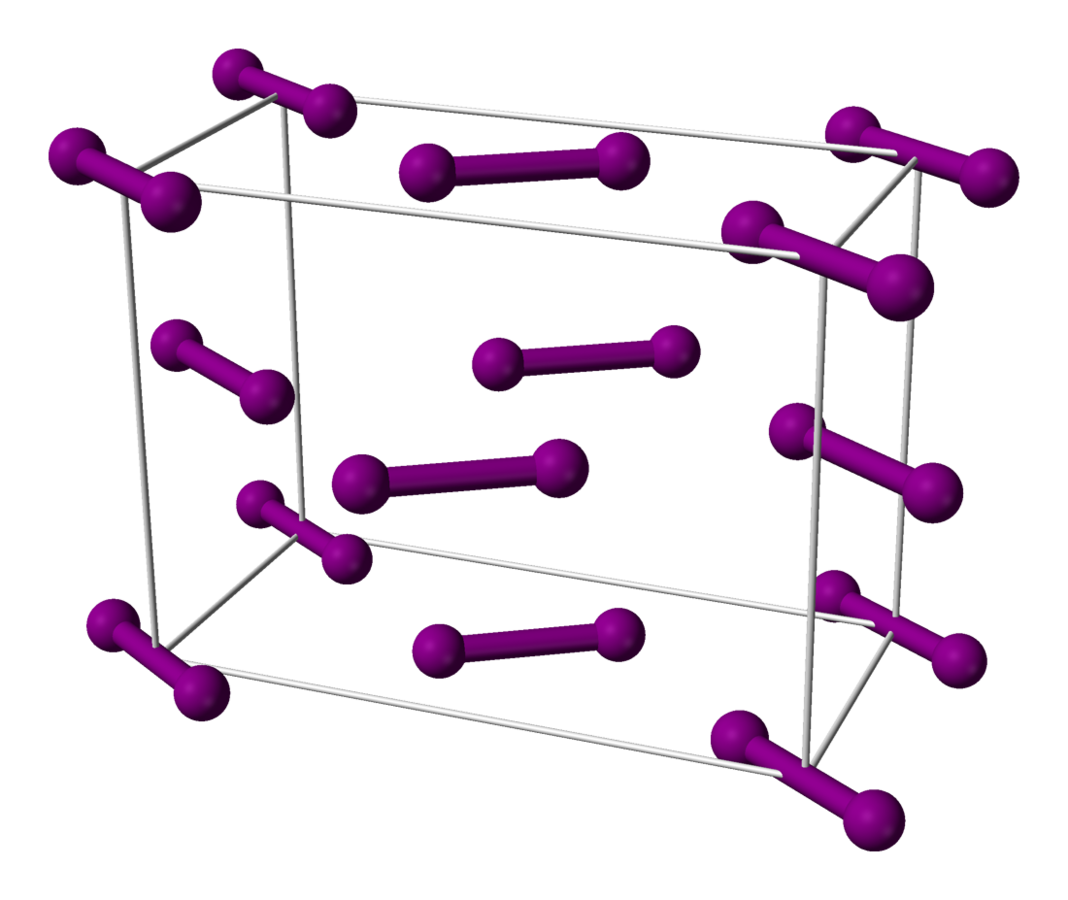
Isolator: alle atomen in de vaste stof hebben octetstructuur;
Het zal dus veel energie kosten om een elektron los te maken!


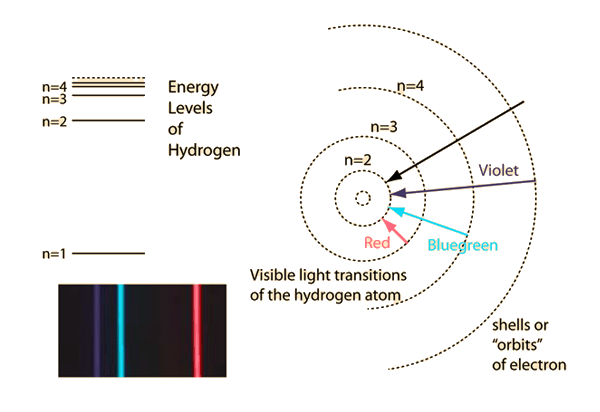
ISOLATOR
GELEIDER
Ionair/covalent
8 VE, geen vrije e-

Metaalbinding
GELEIDER
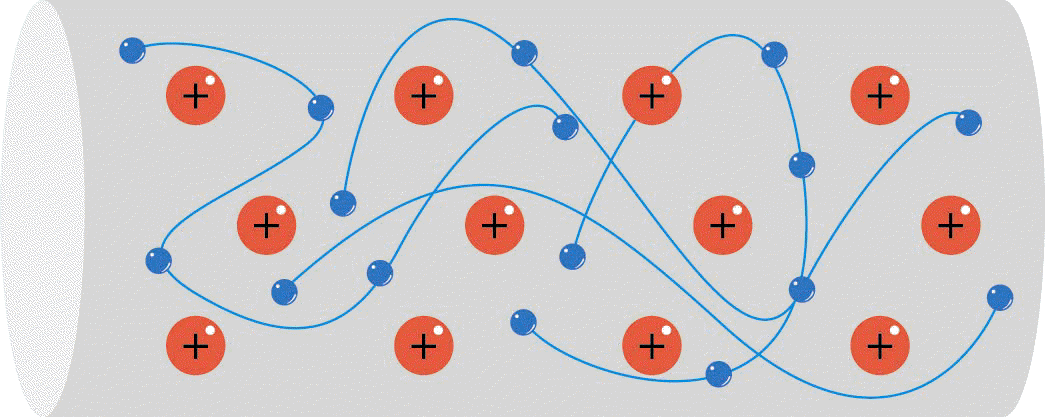
Metaal: valentie-elektronen "over", geen octetstructuur.
Vb. Al-metaal, 3 VE, deze elektronen zijn VRIJ
ISOLATOR
GELEIDER
Ionair/covalent
8 VE, geen vrije e-

Metaalbinding

Wat is nu een halfgeleider?
Grote
bandkloof
Kleine
bandkloof
Geen
bandkloof
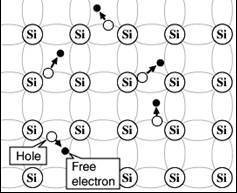
Halfgeleiders
By Anthony Parmentier
Halfgeleiders
- 628



