7 Kaasun tilanmuutos vakiolämpötilassa
FY03 Energia ja lämpö
Ideaalikaasu reaalikaasun mallina
- Verrattuna kiinteään aineeseen tai nesteeseen kaasu on aineen olomuotona erittäin harva ja käyttäytyy tästä johtuen eri tavoin
-
Ideaalikaasu on malli (yksinkertaistus) kaasusta
- Ympäristössä olevat kaasut (esim. ilma) ovat reaalikaasuja
- Ideaalikaasun kaasumolekyylit
- ovat keskenään samanlaisia
- ovat pistemäisiä (ei tilavuutta)
- liikkuvat täysin satunnaisiin suuntiin (lämpöliike)
- törmäilevät kimmoisasti (eivät takerru toisiinsa)
- eivät vuorovaikuta toisiinsa muutoin kuin törmäämällä
- liikkuvat törmäysten välillä tasaisella nopeudella ja suoraviivaisesti
- Normaaliolosuhteissa (NTP) tai niiden läheisyydessä monia kaasuja voidaan tarkastella ideaalikaasuina
- Ideaalikaasun malli pätee parhaiten NTP-olosuhteita korkeammassa lämpötilassa ja alhaisemmassa paineessa
Kuva: Vipu 3 (Otava)
Kaasujen tila ja tilanmuutokset
-
Suljetussa systeemissä kaasun tila riippuu tilanmuuttujista
- Paineesta p
- Lämpötilasta T
- Tilavuudesta V
- Ainemäärästä n
- Yhden tilanmuuttujan arvon muuttuessa vähintään yhden muun tilanmuuttujan arvo muuttuu
- Kaasulait kertovat, miten tilanmuuttujat riippuvat toisistaan
Isoterminen prosessi
- Tilanmuutosta vakiolämpötilassa kutsutaan isotermiseksi prosessiksi
- Lämpötilan T ollessa vakio suljetussa systeemissä kaasun paineen p ja tilavuuden V tulo on vakio
pV = \text {vakio}
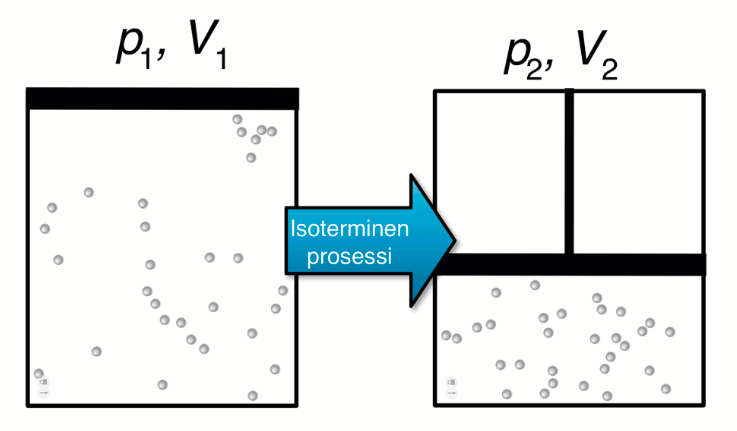
p_1V_1 = p_2V_2
Kuva: Resonanssi 3 (e-Oppi)
Yhtälö alku- ja lopputilanteiden avulla:
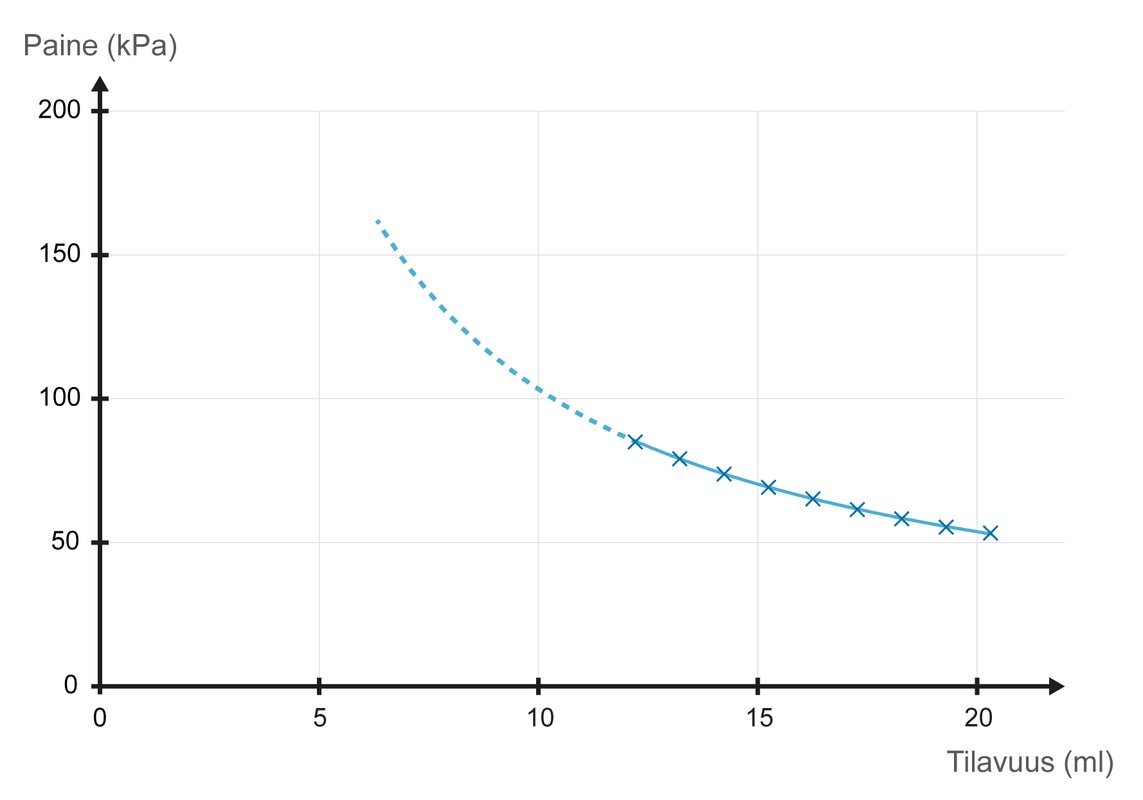
Tilavuuden ja paineen välinen riippuvuus ei ole lineaarista!
pV = \text {vakio}
\Rightarrow \frac{p}{\frac{1}{V}} = \text {vakio}
Mittauspisteet asettuvat nousevalle suoralle, kun piirretään (1/V, p)-kuvaaja.
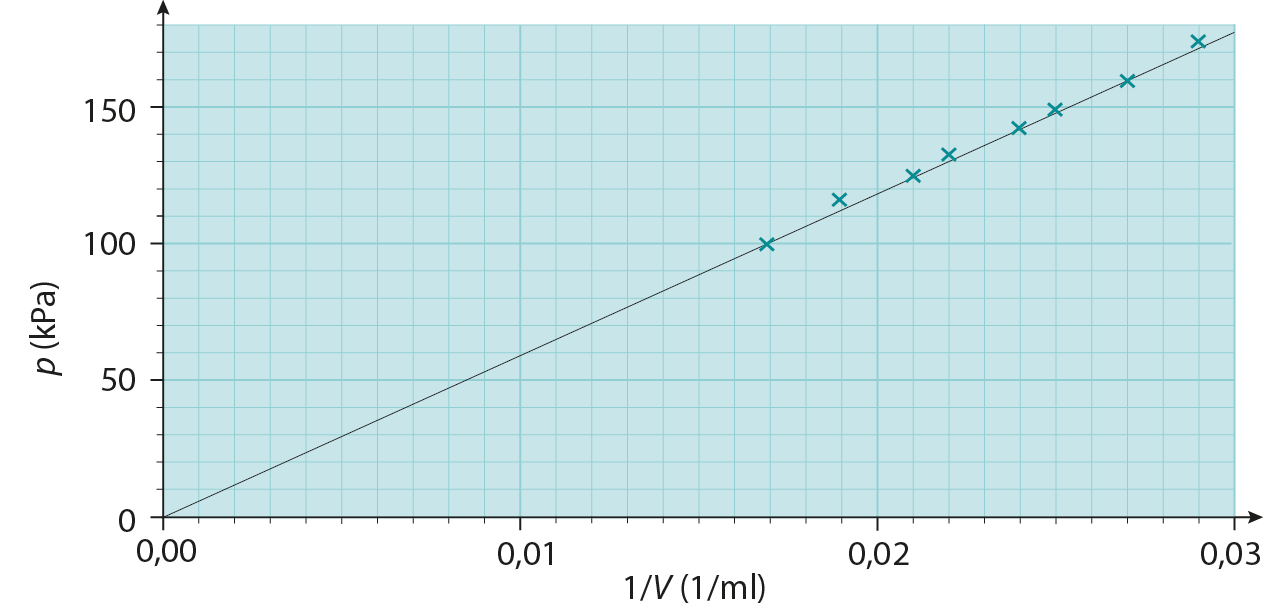
Kuva: Vipu 3 (Otava)
Kuva: Resonanssi 3 (e-Oppi)
Esimerkki 1
Renkaassa, jonka tilavuus on 14 dm³, on 0,30 MPa:n paine. Kuinka suuren tilavuuden ilma vaatisi normaalipaineessa 0,1013 MPa? Lämpötila oletetaan vakioksi.
Kaasun tilanmuutos tapahtuu vakiolämpötilassa eli prosessi on isoterminen. Tällöin kaasun tilavuuden ja paineen tulo on yhtä suuri alku- ja lopputilanteessa.
p_1V_1 = p_2V_2
\text {tilavuus alussa} \ V_1 = 14 \ \text {dm}^3 = 0,014 \ \text m^3
\text {paine alussa} \ p_1 = 0,30 \ \text {MPa} = 0,30 \cdot 10^6 \ \text {Pa}
\text {paine lopussa} \ p_2 = 0,1013 \ \text {MPa} = 0,1013 \cdot 10^6 \ \text {Pa}
V_2 = \frac{0,30 \ \cdot \ 10^6 \ \text {Pa} \ \cdot \ 0,014 \ \text {m}^3}{0,1013 \ \cdot \ 10^6 \ \text {Pa}}
\text {tilavuus lopussa} \ V_2 = ?
V_2 = \frac{p_1V_1}{p_2}
V_2 = 0,0407767 \ \text {m}^3 \approx 41 \ \text {dm}^3
Siispä Boylen lain mukaan
Isoterminen prosessi mikrotasolla
- Kaasun lämpötila pysyy vakiona
- Kaasumolekyylien keskimääräinen vauhti pysyy samana
- Tilavuuden kasvaessa kaasun rakenneosaset törmäilevät harvemmin säiliön seinämiin pinta-alayksikköä kohti
- Kaasun paine pienenee
Isotermit
- (V, p) -koordinaatiston vakiolämpötilakäyriä kutsutaan isotermeiksi
- Mitä suurempi on kaasun lämpötila, sitä suuremmaksi käy kaasun paine, kun tilavuus pienenee
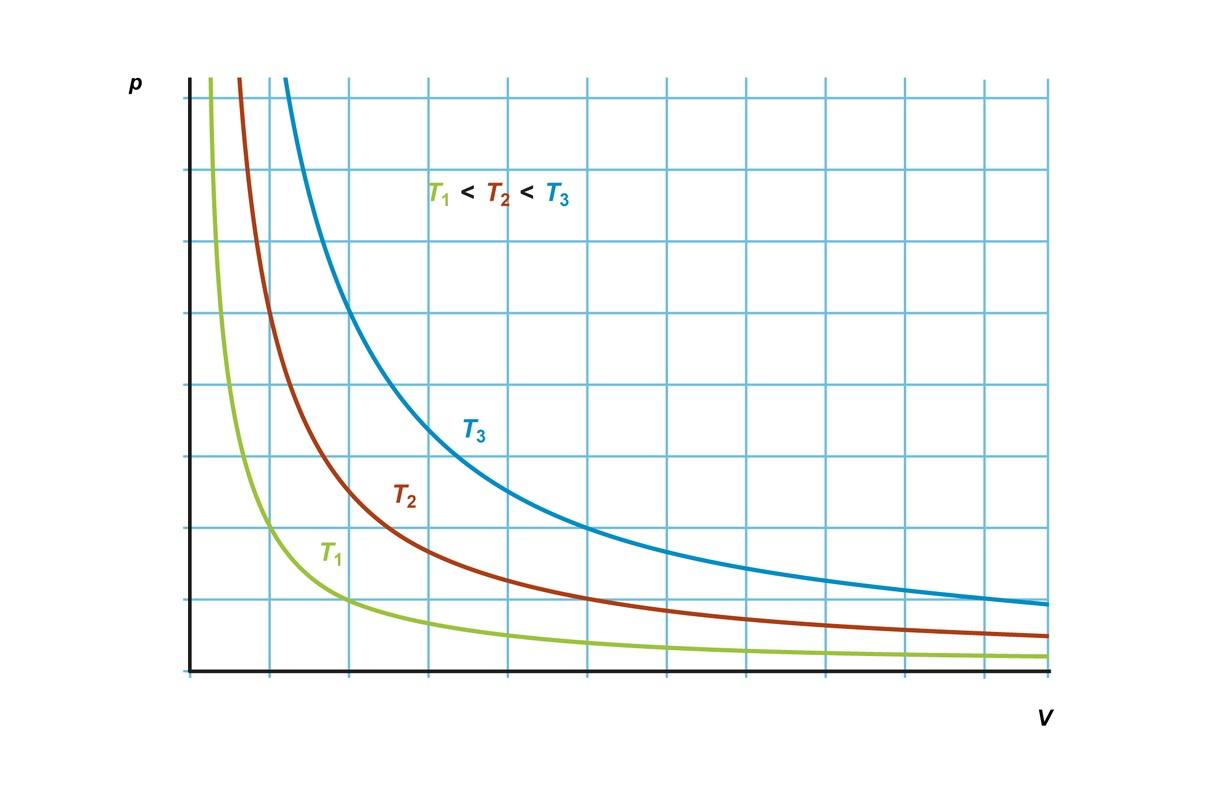
Suuri lämpötila
Pieni lämpötila
Kuva: Resonanssi 3 (e-Oppi)
7 Kaasun tilanmuutos vakiolämpötilassa
By pauliinak
7 Kaasun tilanmuutos vakiolämpötilassa
FY03 Energia ja lämpö
- 139



