9 Ideaalikaasun tilanyhtälö
FY03 Energia ja lämpö
Suljetun kaasusysteemin tilanmuutos
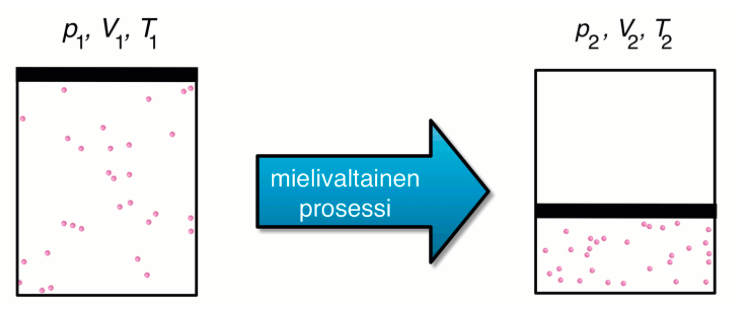
Kuva: Resonanssi 3 (e-Oppi)
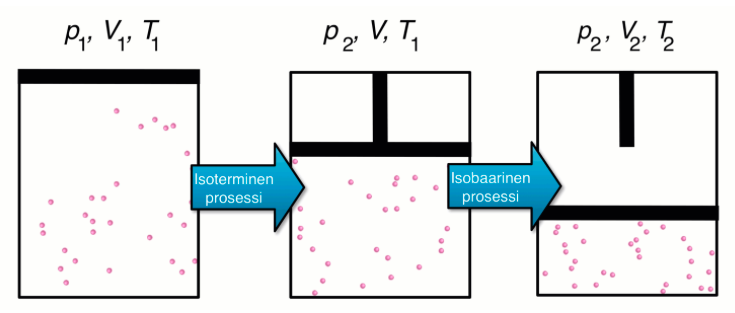
Suljetun kaasusysteemin tilanyhtälö
-
Kaasujen tilanyhtälöt käsittelevät ainoastaan kaasun alkutilannetta ja lopputilannetta
- Niiden välinen prosessi voi olla millainen tahansa
- Suljetussa systeemissä kaasun paineella p, tilavuudella V ja absoluuttisella lämpötilalla T on voimassa seuraava riippuvuus

Laskuissa lämpötila aina kelvineinä!
Kuva: Resonanssi 3 (e-Oppi)
Isoterminen prosessi
Isobaarinen prosessi
Sijoitetaan V Boylen lakiin

Kuva: Resonanssi 3 (e-Oppi)
Esimerkki 1
Heliumilla täytetty säähavaintopallo voi laajeta 3,0 m³:n tilavuuteen ennen halkeamistaan. Säätilaa tutkitaan palloon asennetun lähettimen avulla korkeudella, jossa paine on 710 hPa (noin 3 km) ja lämpötila –12 °C. Pallo täytetään normaaliolosuhteissa (NTP).

Mikä on tilavuus, johon pallo voidaan täyttää, jotta tiedon hankinta tuolta korkeudelta onnistuisi?
Säähavaintopallo muodostaa suljetun kaasusysteemin, joten kaasun ainemäärä ei muutu. Suljetun kaasusysteemin tilanyhtälön mukaan
Avogadron laki
- Aikaisemmin tarkastelluissa kaasulaeissa kaasun määrä on ollut vakio (suljettu kaasusysteemi)
- Myös kaasun määrän muutos vaikuttaa tilanmuuttujiin p, T ja V (avoin kaasusysteemi)
- Avogadron laki: samassa tilavuudessa V, lämpötilassa T ja paineessa p kaikki kaasut sisältävät saman ainemäärän n eli yhtä monta kaasumolekyylia
- Yhdessä moolissa kaasua on Avogadron vakion verran rakenneosia
- Ainemäärä n voidaan laskea aineen massan m ja moolimassan M avulla
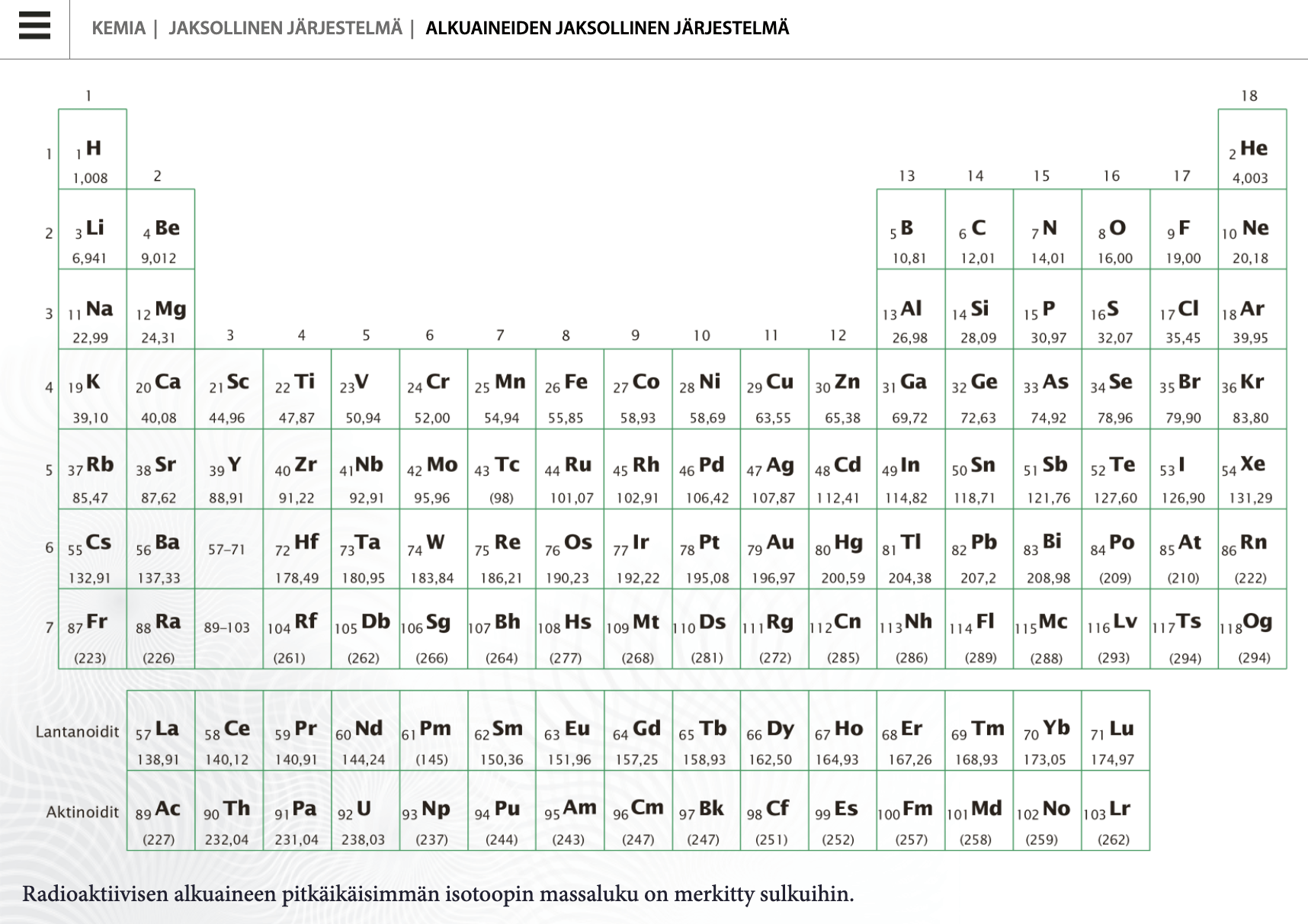
Kuva: MAOL-taulukot (Otava)
Yksittäisen atomin moolimassa on merkitty jaksolliseen järjestelmään yksikössä g/mol
Jos molekyylissä on useita atomeja (esim. O2 tai H2O), pitää moolimassa laskea itse
Yleinen ideaalikaasun tilanyhtälö
- Avogadron lain mukaan kaasun tilavuus on suoraan verrannollinen ainemäärään (V ~ n), joten
- Tämä vakio on sama kaikille kaasusysteemeille, sitä kutsutaan mooliseksi kaasuvakioksi (yleinen kaasuvakio)
- Paineen, tilavuuden, lämpötilan ja ainemäärän välinen riippuvuus on nimeltään kaasun yleinen tilanyhtälö (ideaalikaasun tilanyhtälö)
Esimerkki 2
Vappupallon tilavuus on 11 litraa 19 °C lämpötilassa. Pallossa olevan heliumin massa on 2,0 g. Laske vappupallon sisällä vallitsevan paineen suuruus. Pallon kimmo-ominaisuuksien muuttumista (venymistä tai puristumista) ei oteta huomioon.
Lasketaan nyt heliumkaasun paine ideaalikaasun tilanyhtälöllä
Heliumkaasun ainemäärä on
9 Ideaalikaasun tilanyhtälö
By pauliinak
9 Ideaalikaasun tilanyhtälö
FY03 Energia ja lämpö
- 102



